睡眠是人类生活中必不可少的内容。其重要性就如世界卫生组织的一份报告中所言,“睡眠和空气、食物、水一样,是人类生活的基本必需品”。不少专家都认为,成年人每夜至少要睡7到9个小时。没有足够的睡眠会损害人的身体健康也会带来一些其他的问题。所以拥有足够的睡眠非常重要。但是,在现代社会里,失眠是许多人面临的重要生活问题之一,失眠原因多种多样,对睡眠的深入了解是解决相关问题的重要途径之一。
但是,当今人们对睡眠的理解主要是基于EEG信号的睡眠分期,对其基础水平的脑网络动态特性却知之甚少。来自牛津大学精神病学系的研究人员对这一问题进行了深入挖掘,并使用高分辨率的fMRI结合睡眠监测EEG技术(PSG)对这一问题进行了研究,相关研究成果发表在《Nature Communications》。
本研究利用功能磁共振来探索觉醒-睡眠循环的全脑时空综合特性以及全脑网络状态的变化过程。为了无偏倚的评估全脑网络活动所经历的状态是如何随着睡眠循环所演变的,作者使用隐马尔可夫模型对57个正常被试的神经影像数据(有效使用数据18个)进行了数据驱动式的分析。这些被试在采集功能磁共振数据的同时也采集EEG信息。
作者采用的隐马尔科夫模型有助于发现清醒——(至)非快速动眼睡眠循环期间不同脑网络状态的动态特性。作者的结果揭示了每个睡眠周期内部以及不同睡眠周期之间的脑网络关键转变轨迹,同时强调了N1睡眠期以及睡眠期前后觉醒期的异质性。
读前小知识之隐马尔科夫模型(HMM)是什么?
如果你做自然语言处理,隐马尔科夫模型肯定是必听过的统计模型之一,如果你以前了解也没关系。读完这篇科研论文章,你应该就能体会它的优点所在。隐马尔科夫模型是关于时序的概率模型,描述由一个隐藏的马尔科夫链随机生成不可观测的状态的随机序列,再由各个状态生成一个观测而产生观测随机序列的过程。是不是听不明白?我也看不明白这段话,我们换个思路看。
HMM(隐马尔科夫模型)能干嘛?输出来的东西解决个什么问题?
隐马尔科夫模型是从马尔科夫模型发展而来,它解决是一个随着时间变化观测对象出现随机变化的过程问题,也就是说使用这个模型,你可以描述一段随机变化的进程。举个例子(这个例子不是我的,是引用的,也是我目前见过解释隐马尔科夫模型最简单的方式):我们通常都习惯寻找一个事物在一段时间里的变化规律(这是我们希望在这个世界中能够简化对世界的认识,抽象出对客观规律认识从而对世界进行改造的重要途径)。在很多领域我们都希望找到这个规律,比如计算机中的指令顺序,句子中的词顺序和语音中的词顺序等等。
但是,很多规律都不是在显象观察中就可以得出的,比如说对天气的预测,假如我们使用观察到的植物海藻的表现来预测天气的状态变化,这种观察的表象是看不到天气变化这个隐藏起来的规律的,但是我们是可以通过对海藻在一段时间内的表现的变化状况来预测分析天气的变化状态,在这个过程中,一个能够用来从表象的海藻变化来描述隐现的天气变化的统计模型我们就可以称其为:隐马尔科夫链。(精彩的比喻和概况,有助于您的理解)
一般来说,天气的阴晴状态与红绿灯不同,我们不能确定下一时刻的天气状态,但是我们希望能够生成一个模式来得出天气的变化规律。我们可以简单的假设当前的天气只与以前的天气情况有关,这种假设呢被称为马尔科夫假设。也就是说马尔科夫假设是一个关于当前状态发生的概率与该事物在其他状态发生时的发生概率存在一定关系的概率假设,当前概率与该事物在n个状态下发生时的概率存在关系,就可以称之为n阶马尔科夫模型。但是呢,我们并不是总有机会直接去观察其他状态的,比如生活在海底的鱼人小姐姐(一个美丽的传说)牵挂她在陆地上的小哥哥,但是她被她的坏老爹(不开明)给囚禁了,没法去观察海上的天气,她只能通过观察窗外的海藻的变化状态来推测下一天的天气状况。这种情况下,她观察到的海藻的不同状态是难以对应于不同的天气状态的,也就是说可能x个海藻状态对应的是同一种天气状态,在这个过程中通过其他状态来预测当前状态就会多出一层关系:表象(即海藻状态)状态所反映的隐含状态(即天气状况)的概率分布,这一层我们可以假定它叫隐含转换概率(我造的啊,为了便于理解)。那么现在我们有两个状态了,第一是海藻的所有状态,第二是天气的所有状态。同时,我们有了三种发生概率,第一是海藻状态的发生概率,第二是海藻所对应的天气状况的发生概率,第三是天气状况的发生概率。根据这样的建模,我们就可以根据观察的表象来估计隐象的发生概率(预测问题也称解码问题),也可以根据已有的表象数据和隐象数据来构建HMM,评估某一个状态符合HMM状态的概率(评估问题)。最后,它也能利用观察到的表象数据来构建一个HMM(隐马尔科夫模型)来描述这种发生关系,也就是学习问题(这个是最难的)。
最后附上学习网址,感兴趣的同学去看哦!http://blog.sciencenet.cn/blog-641976-533895.html
研究背景
人们对睡眠期大脑的理解多数是基于低空间分辨率的EEG或者相应的技术。对睡眠的一个核心的行为理解是,人们缺乏对周围环境的互动和应答,例如觉醒水平的减低。缺乏跟处于睡眠的被试的交流意味着作者要依赖生理记录来科学的描述睡眠和睡眠的分类分期。
当前先进的神经影像技术和网络分析方法被用来刻画清醒时的脑活动。但是,作者对睡眠时大脑的理解仍然是基于仅有少数通道的EEG记录。当今对正常睡眠的研究主要依靠多导睡眠图技术(PSG,也依赖EEG),以及肌电图(EMG)、眼点图(EOG)、心电图(ECG)以及呼吸检测。依靠EEG简单的几个电极和视觉上的频谱特征就把人类的睡眠分为清醒期、非快速动眼睡眠期(包括N1、N2和N3期)。这种分期始于20世纪30年代的技术。
PSG是研究睡眠的必要手段,但是它可能不能全面的反映人脑的活动。PSG无疑是最快速且最简单的方式来确定一个人的觉醒水平。虽然源头来自EEG的PSG睡眠分期仅仅可以当作是觉醒阈的一个替代指标,但是随着时间的推移许多人愿意认为它或多或少的反映详尽的全脑活动状态。然而,以下两点让作者对它是否能反映全部脑活动产生了质疑:一是固定30秒的计分窗,二是EEG的电极少,以至于它反映的是时空上平均的脑活动。另外,PSG与被试的睡眠主观感受相差甚远。这一点对于失眠患者来说尤为重要,因为失眠的临床诊断不完全依赖PSG,很多时候是根据患者主观感受。
神经影像技术可以更加精巧的研究睡眠周期时的人脑活动,但是大部分研究都摆脱不了对低空间分辨率的PSG的严格依赖。全脑神经影像先包括功能连接、结构连接、任务态相关脑网络以及计算模型等能更好的研究脑活动。然而多数研究都严格的依赖PSG技术,即——将PSG的睡眠分期与功能脑数据做回归分析。这种分析探测到了PSG与睡眠图素关于激活脑图、功能连接模式、图论指标以及EEG微状态等方面的关系。然而,这种方法从上至下受PSG约束的分析,损失了高分辨率神经影像的许多有用信息。
本研究的目标和内容简述:
本研究摆脱了对传统睡眠分期定义的束缚,作者的目标是利用全新的数据驱动方法来阐明全脑网络变化状态,以此能补充甚至扩展当前作者对经典睡眠知识的理解。受到个体PSG分期能够被fMRI信息所确定的启发,作者采用隐马尔科夫链模型(HMM)来分析57个正常被试的BOLD信号(最终采用了18个拥有完整PSG分期状态的由fMRI得到HMM状态的数据),来探索睡眠周期循环期间的大尺度脑网络。同时,作者也采集被试的EEG信号(因为需要与传统PSG睡眠分期进行比较分析)。
HMM允许作者不受PSG分期的约束,来直接的从fMRI数据上探测睡眠周期循环期间的人脑网络状态的转化。而且,这种状态转化是同时在秒级别(核磁的TR时间尺度)的时间尺度上,以及毫米的空间尺度上进行的。相较于其它动态功能连接分析方法,HMM框架能明确的估计推断状态间的转化概率(也就是我们在前文中提到的隐含状态关系)。作者的结果表明这些信息(fMRI)能被用来发现睡眠相关的新的全脑活动信息,对PSG推断的传统脑活动分期提供了必要的来自于高空间分辨率研究的补充。
研究方法
fMRI和PSG数据的采集和处理:
fMRI数据采集使用3.0T西门子扫描仪,T2*加权的平面回波序列,参数如下:TR=2.08s,TE=30ms,matrix=64*64,体素大小为3*3*2mm3, FOV=192mm2,1505个采集点。
fMRI数据处理利用SPM8完成。预处理包括头动校正、空间标准化到MNI空间以及空间平滑(高斯平滑核,FWHM=8mm3)。数据降采样到4*4*4mm的分辨率。通过RETROICOR方法(一个2000年发表的用来估计生理噪声的工具)估计ECG记录的心跳及呼吸相关的噪声,同时回归掉头动参数。接着,对数据进行带通滤波(0.01-0.1Hz)。
同时进行的PSG信号采集通过EEG,EMG,ECG,EOG,脉搏血氧饱和度与呼吸进行记录。EEG:30通道脑电帽,FCz电极作参考,5kHz采样率,低通滤波为250Hz。
MRI以及波动伪影校正基于平均伪影减除法执行(VisionAnalyzer2)。EMG,ECG和EOG:采样率为5kHz,低通滤波为1kHz。脉搏血氧测定采用三重扫描仪,呼吸采用磁共振兼容设备。
HMM方法:
HMM(隐马尔科夫模型)应用在90个ROIs的时间序列上(AAL模板),从而以数据驱动的方法解析fMRI信号中的动态脑网络。作者使用FSL软件中的fslmeants函数提取90个ROIs的时间序列(每个ROI的时间序列由此ROI内所有的体素的平均时间序列计算得到),并对其去均值且除以标准差(z标准化),最后将所有被试的数据在时间维度上拼接起来,形成90*(57*1500)的数据矩阵。HMM分析采用Matlab工具箱HMM-MAR(一个专门用来对网络数据构建变化特征的HMM工具包,同附上网络链接https://github.com/OHBA-analysis/HMM-MAR)来操作。
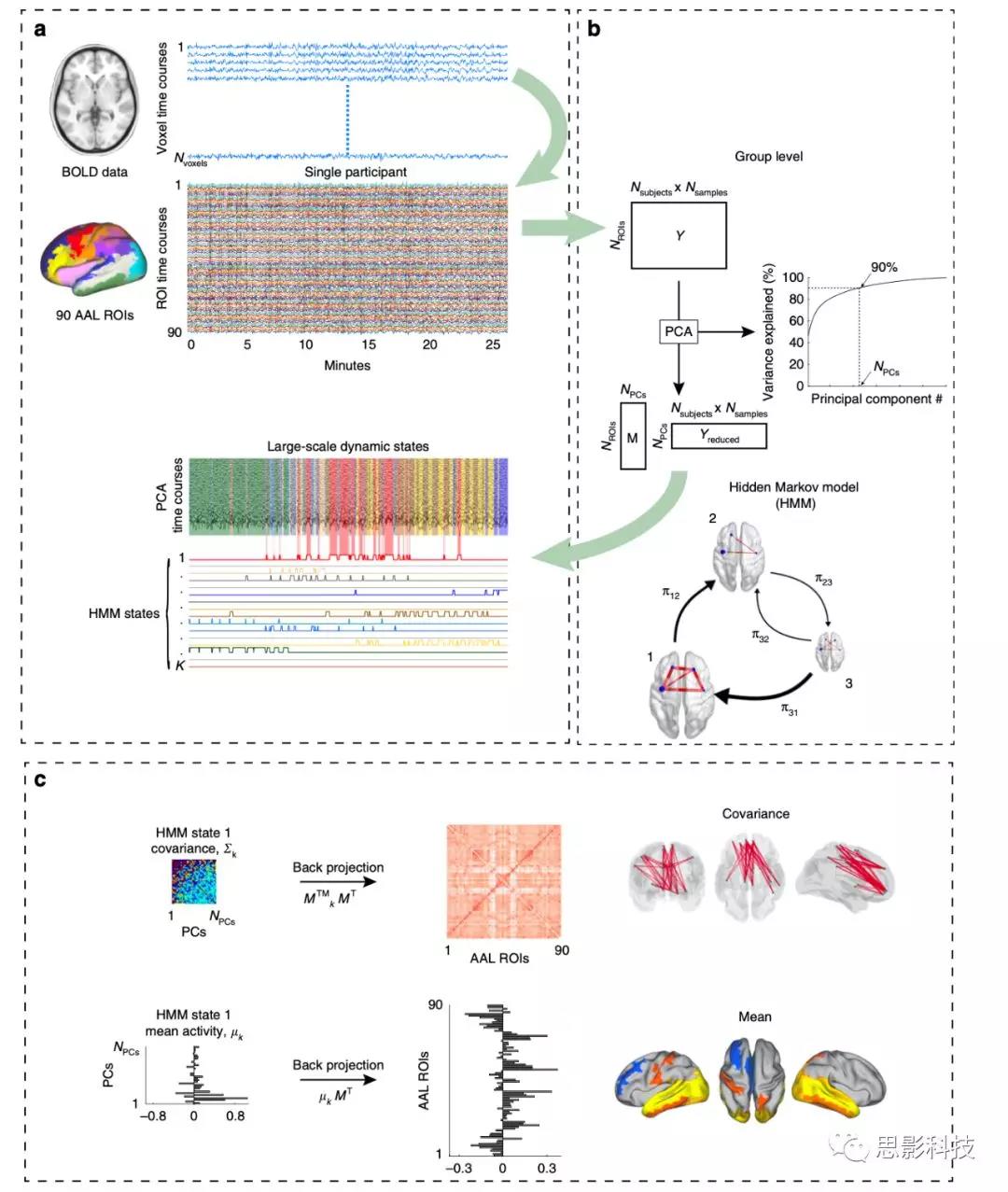
图1. 使用马尔可夫模型在睡眠记录的同时从fMRI解析的动态脑网络。
a ROI时间序列从AAL模板中提取。每个ROI时间序列都经过z标准化。
b 所有被试的数据拼接,并使用PCA进行降维,并保留90%解释方差的前25个主成分。HMM对25个主成分时间序列进行分析,得到k个脑网络状态(即二阶统计),每个状态都有个一个相对应的时间序列(即一阶统计),每个时间序列描述每个状态时活动或不活动的时间点。
c 每个HMM状态由多元高斯分布所刻画,其包括一个功能连接矩阵和一个平均分布。最后各个HMM结果反投射到原始的空间(通过前面得到的PCA混合矩阵)。
结果
HMM(隐马尔科夫模型)确定的全脑网络状态。
具体方法请见方法部分,具体细节可以参考全文计算得到的HMM包含一系列全脑网络状态,每一个状态由一个多元高斯分布确定,其包括:
(1)一个平均激活(静息态用脑活动更准确)分布,代表一个状态激活时每个ROI的平均活动水平。
(2)一个功能连接矩阵,其汇总了特定状态时ROIs时间序列间的共激活关系(即功能连接)。HMM也包括一个状态转换的概率矩阵。每一个状态也对应着一个时间序列,其描述的是状态激活时的时间点(比如第5,6,7,8,11个时间点时处于第1个状态,那么此状态的时间序列在这5个时间点拥有一个概率值,而其它时间点的概率值为0;如图2.a)。HMM确定了19个脑网络状态,关键的是,HMM没有借助任何PSG分期的信息(因此HMM状态是完全基于fMRI数据得到的)。
当把HMM的结果与PSG分期的结果进行比较时,为了得到无偏倚的被试内统计测试,作者只调查了一部分HMM的结果,即18个拥有所有PSG睡眠分期的被试(只有这18个患者在扫描期间56分钟内完全经历了清醒期、N1、N2、N3期)。
PSG睡眠分期的脑网络状态基础。
通过HMM仅从fMRI信息推断得到的19个脑网络状态包含了绝大多数PSG分期的动态信息。上述18个被试的HMM状态的时间序列以及PSG信息在图2.a中展示。图2.a展示了HMM不同状态的激活与PSG分期的共变关系。图2.b展示了通过多元方差分析(MANOVA)将PSG分期投射到HMM状态的时间序列空间的结果。从图2.b可见清醒期(W)和N1睡眠期显著的跟N2睡眠期分离,它们三者进一步与N3睡眠期分离。
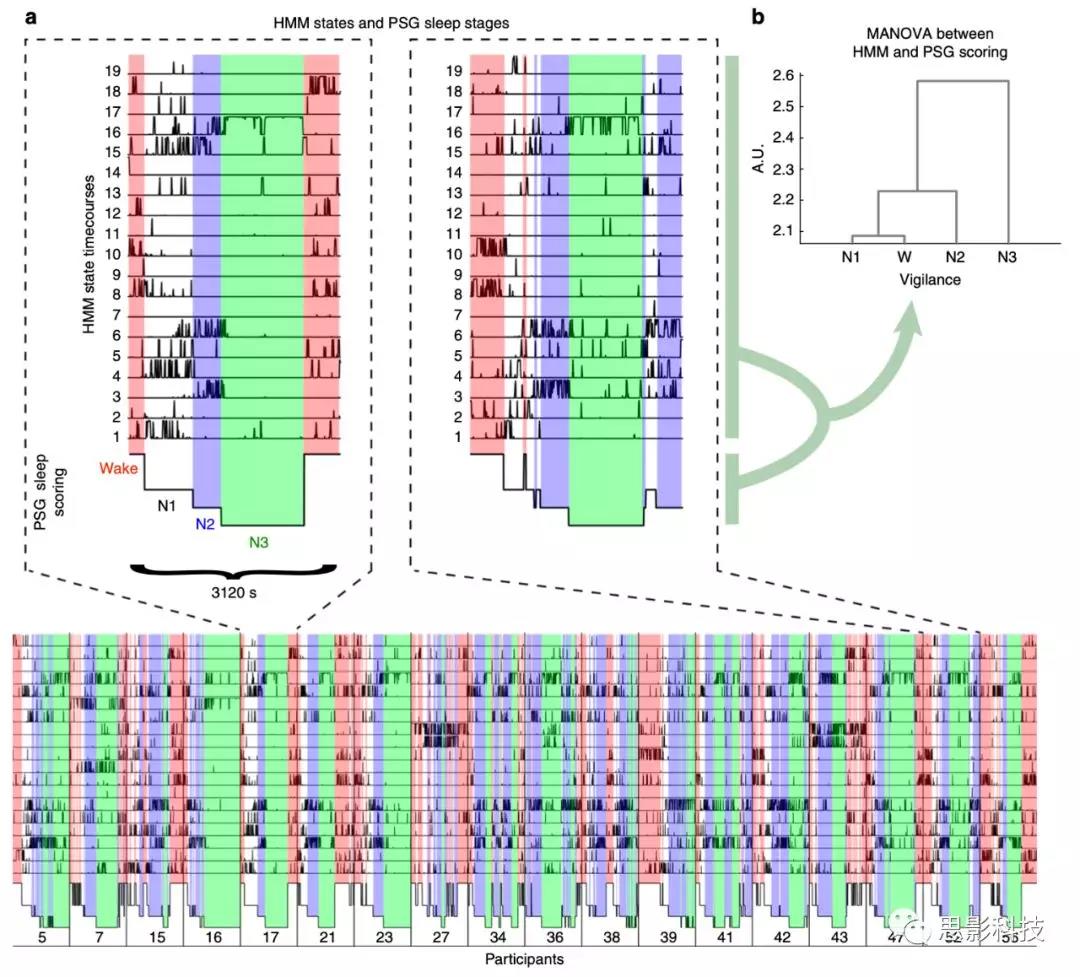
图2 HMM状态的时间序列以及它们和PSG的关系。
a图展示了19个状态的时间序列,表示18个人的每个状态在每个时间点激活时的概率。a图下面展示的是独立记录的PSG睡眠评分。覆盖在图上的不同颜色表示的PSG睡眠的各个分期。两个虚线框表示两个人的样例。HMM状态中有些人的状态很零星,但是只出现几个人身上。
b图展示了HMM状态和PSG分期的多元量化关系,其揭示了对HMM状态的层次聚类分组。
全脑网络可以定义不同的PSG睡眠分期。
接下来,作者检验了被试全脑网络状态对上述HMM(隐马尔科夫模型)状态与PSG睡眠分期多元关系的贡献。作者量化了HMM状态在每一个PSG睡眠分期中的敏感性和特异性。某个HMM状态在每一个PSG睡眠分期中的敏感性定义为该睡眠期中某个HMM状态的激活的总时间点数占该PSG分期所有时间点的比例。特异度定义为在一个特定PSG分期中发现某个HMM状态激活的似然比。
作者使用配对t检验以及PSG得分的随机化方案比较了敏感性和特异性。图3.a和b展示了统计的结果。HMM8、10以及18状态在清醒期的敏感度和特异度都很高。HMM3和6状态在N2期,以及HMM16状态在N3期的敏感度和特异度都很高。但是在N1睡眠期却没有敏感度和特异度都很高的HMM状态。
总体来说,清醒期与多个HMM脑状态相对应,而N2和N3期与特异的几个脑状态相对应。相反,N1睡眠期是一个包含很多HMM脑状态的混合期。
PSG睡眠期间全脑网络动态的变化。
如图3.c所示,在N2和N3期有着高特异度的脑状态(HMM3、6和16)通常表现为更长的寿命(相较于清醒期和N1期)。状态寿命从几秒到几十秒不等。图3.d和e展示了两个动态特征,一是总HMM状态切换次数,二是独特HMM状态的范围。清醒期和N1期的两个指标都明显比N2和N3期高。有趣的是,N3期的切换次数特别低。
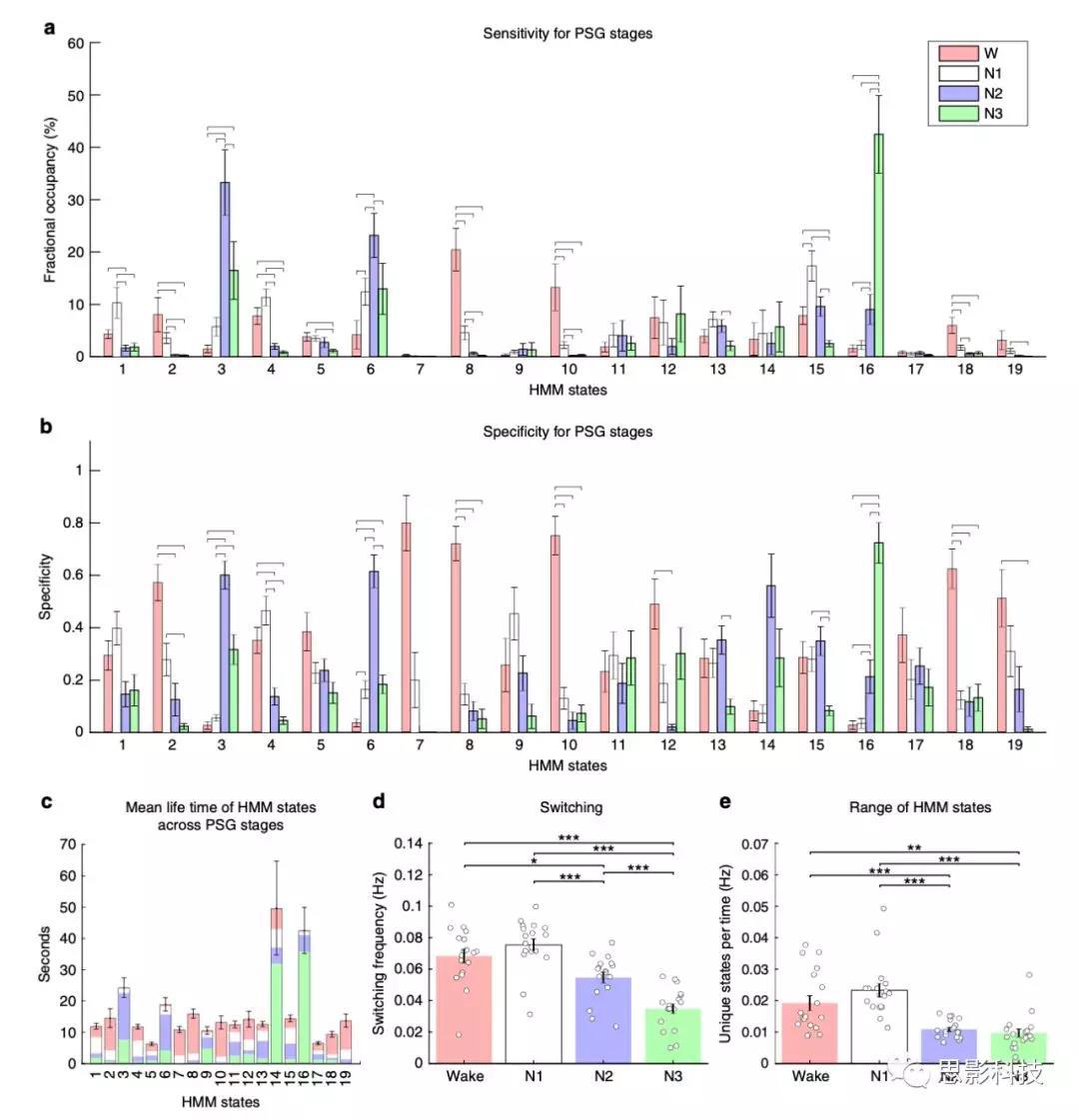
图3 PSG各个分期内HMM状态的敏感度和特异度以及动态特性。
a 19个HMM状态的百分数占比。
b HMM状态的相对于PSG的特异度。柱子表示的组平均数,误差线表示标准误。ab图中的水平线表示有统计学差异(p<0.01以及置换检验)。
c表示19个HMM状态平均寿命时间。误差线表示标准误。各个颜色的高度表示其在各个PSG睡眠分期的特异度。值得注意的是:拥有长N3短N2的状态(14和16)平均寿命最长。
d展示了各个PSG分期内HMM状态的转换频率。
e展示了各个PSG分期中不同的HMM状态的频率(HMM状态数/PSG分期内总的激活时间点数=每个时间点有几个不同的状态存在)。de中的误差线表示标准误。从de图可知,清醒期和N1睡眠期的动态性最强,而睡眠N1期和N3期的动态性较弱。
PSG定义的睡眠周期可以表达为全脑网络状态转换的一种模式。
以上的分析都是从PSG睡眠期出发的。现在作者反过来,从HMM状态出发来思考作者的结果,看看HMM状态的结果能不能得到潜伏在PSG背后的睡眠周期的一些新的发现。图4展示了19*19的脑网络切换概率矩阵(共19个HMM状态构建出来的)。这个矩阵被用来进行模块化分析。通过考虑HMM(隐马尔科夫模型)状态间最大的转换频率,阈值化的转换矩阵可以归纳为4个转换模块(图4.c)。具体的解读见图4。总体来说,用HMM定义的大脑网络的状态转换过程跟PSG定义的睡眠周期有一个很好的契合。
值得注意的是,一系列有着多种PSG睡眠周期的HMM状态形成了互相高转换率的模块(HMM状态1,4,15)。这个模块介于清醒期和N2、N3睡眠期之间。
另一个有趣的结果是,对PSG清醒期特异度高的模块可以分为两个亚模块,分别是红色模块和黑色模块。通过进一步分析,发现黑色模块在WASO(睡眠之后的清醒期)的特异度和敏感度都较高。因此,作者推测黑色模块可能代表WASO,而红色模块代表睡前清醒期。
尽管转换概率图提供了清醒到睡眠的多条通路,但是作者应该注意到HMM8直接到HMM15这条通路,而且应该注意到HMM15总是守护着通往N2/N3睡眠的蓝色模块。同样的也应该注意到觉醒通路相关的HMM4到HMM10,以及HMM10与黑色WASO(睡眠之后的清醒期)模块的相同。进一步,作者更加应该重视对N2期特异的蓝色模块内的三角转换关系。
总的来说,HMM定义的全脑网络状态转换为作者提供了很多PSG评分得不到的信息。比如数据驱动得到的N1睡眠,WASO(睡眠之后的清醒期)相关的全脑网络状态以及清醒期和睡眠互相转换的多条脑网络状态通路。
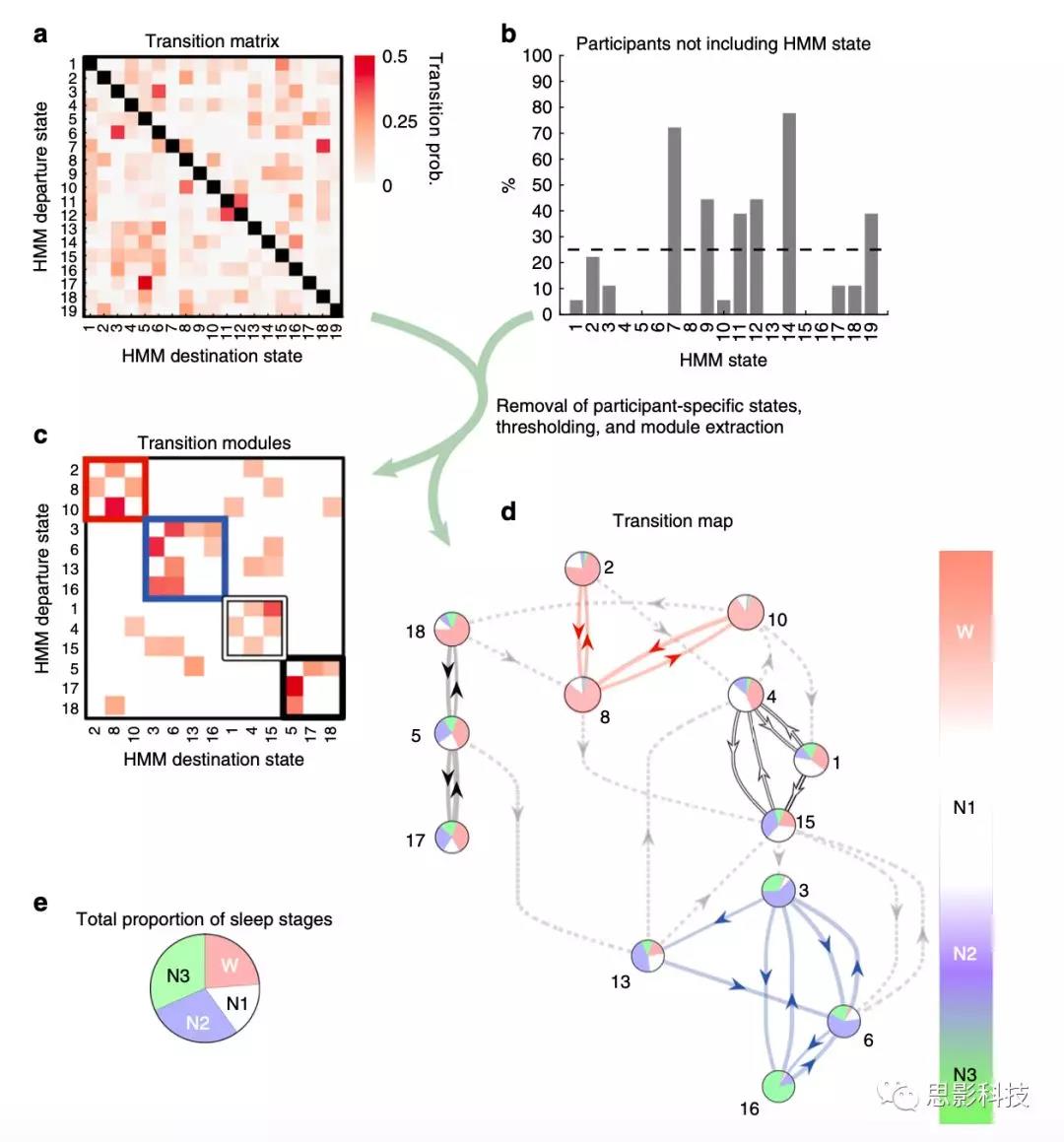
图4 HMM脑网络状态之间转换的模块分析。
a 19*19的状态转换概率矩阵,量化了状态与状态之间转换的似然。
b部分状态散落在少数被试(很多人没有这个状态)。25%的人没有这个状态的,被排除。
c互相转换频率最高的状态组成一个模块。
d c中状态展示为饼图,表示在各个睡眠期的特异性。箭头表示的是状态流动的方向,线条的粗细表示转换概率。d图描述了HMM状态的流动通道信息,从最顶端的清醒期最高活动,下降到N1期,再到N2以及N3。有趣的是清醒期拥有两个模块,一个是红框一个是黑框。尽管N1期没有特异性的HMM状态,但是N1期确实处于清醒期和N2、N3期之间。
e 饼图表示PSG各个期的比例。
脑网络状态的空间激活图以及FC图。
图5和图6展示了平均激活图。FC图在辅助材料里面有展示。图5.a重点: 1、HMM8状态的DMN和一个被作者称为ACN网络的网络(anti-correlation network,前馈网络,主要是dLPFC区域)呈反向关系。
2、清醒期高级网络活动明显。图5.b重点:1、HMM18和HMM8激活分布一致,但是关系相反(即DMN负激活,ACN正激活)。
3、HMM5和17发现额叶正激活,这与以往的研究一致,表明从睡眠清醒的过程中额叶会激活。图6.a为与N1睡眠相关的脑区激活图,主要结果为:皮下区域与初级感觉皮层的反向激活关系。图6.b为与N2睡眠相关的激活图,主要结果为:辅助运动区域参与到这个睡眠期的各个HMM状态,而且这些激活区域与以往的睡眠纺锤波的fMRI相关脑区重叠。但是,没有哪个HMM状态是单独的被睡眠纺锤波或者K复合波驱动的。图6.c展示了HMM16状态的激活图(占N3睡眠的大部分时间),主要结果:中央旁小叶和邻近的辅助运动区域局限性的激活增加,而两侧颞中/上回、眶额叶、顶下小叶顶盖部、两侧岛叶以及内测颞叶激活减低。

图5 清醒期的平均激活图。
A图展示的是睡前清醒期的3个状态时的脑激活图。HMM8时DMN激活并伴随着DAN/CEN的去激活,这个现象提示了DMN和ACN的反向关系。
B图展示的睡后清醒期的3个状态时的脑激活图。HMM5和17时额叶激活明显。DAN/CEN=背侧注意/中央执行网络。
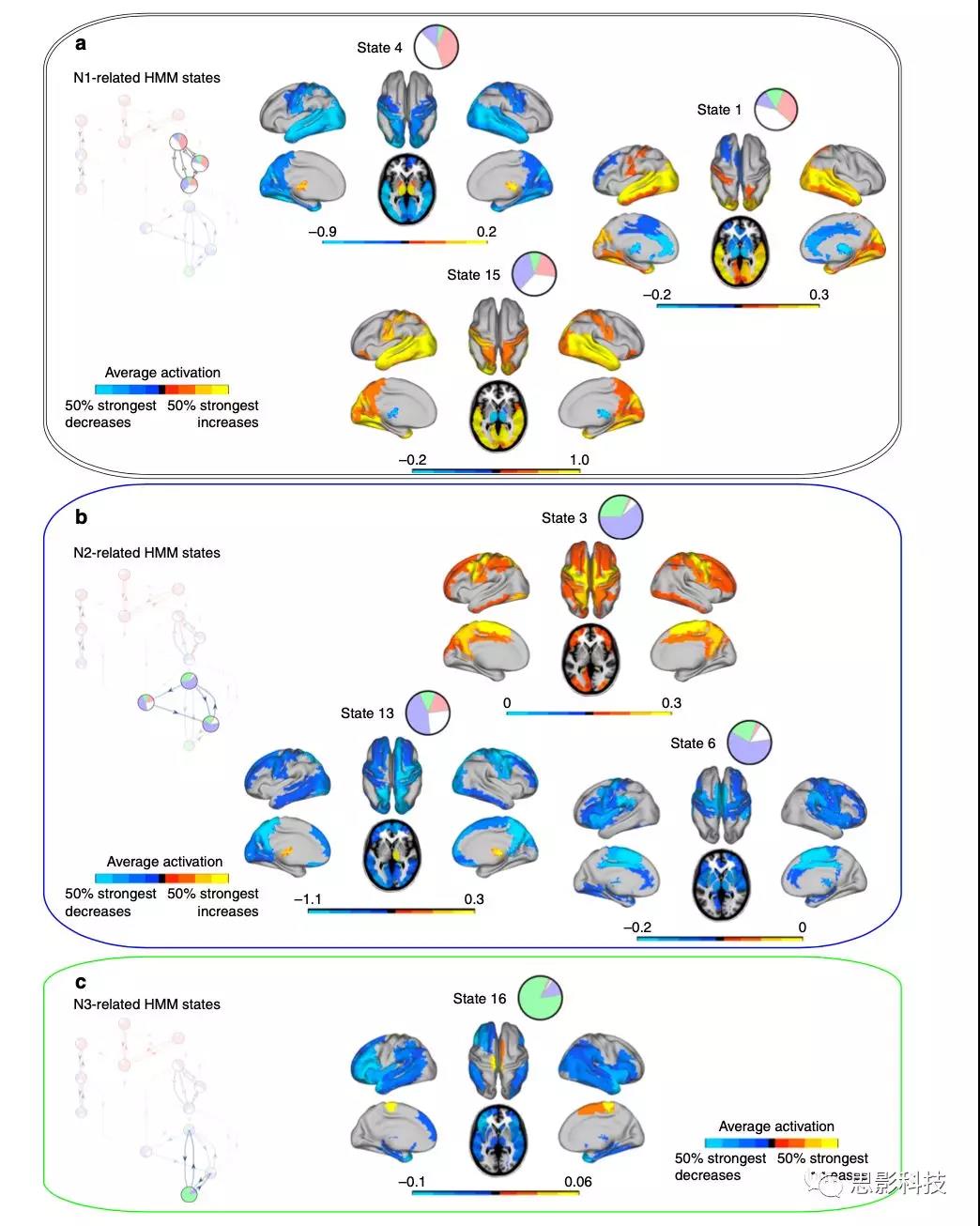
图6 睡眠相关HMM状态的平均激活图。
a N1睡眠的HMM状态的平均激活图,主要激活区域是皮层下区域以及初级感觉皮层。
b 与N2睡眠相关的3个HMM状态时的激活图。HMM3和6在以往研究中与睡眠纺锤波相关的脑区有着最高的正和负激活。
cHMM16主导了慢波睡眠(N3)。有趣的是,这个状态显著特征是额叶和岛叶的激活减低,而辅助运动皮层和中央旁小叶局部脑区的激活增加。
讨论
通过对大尺度脑网络以及脑网络的动态特性进行数据驱动分析,作者探索了健康人类清醒-非快速动眼睡眠循环期间人脑活动的动态的时空模式。作者不依赖传统的PSG定义的睡眠分期,而是使用HMM提取了19个反复出现的全脑网络状态。而且这19个状态是由平均的BOLD激活、功能连接以及每个时间点激活的可能性所定义的。通过将HMM定义的脑网络状态转换与PSG得分进行对比,作者发现了传统PSG分期下脑网络动态的基础。HMM定义的状态转换的时间分辨率是在秒水平进行,提供了对传统PSG分期的精细描述。关键发现是,对HMM状态转换概率的仔细检测进一步揭示了睡眠周期中大尺度脑网络活动的异质性,这是PSG分期不能捕捉到的。
本文最核心的讨论部分为图7的解图,因此先重点解读图7作者想表达的内容。图7是HMM定义的脑网络状态的转换概率图,而且通过模块分析将脑网络状态有机的组织在一起。清醒期、N2睡眠以及N3睡眠期分别被表征为一个和多个脑网络状态,与PSG分期形成一个很好的对应关系。相反的是,没有哪个脑网络状态与N1睡眠有着良好的对应关系,即特异度不高。另外,睡眠前的清醒期与睡眠后的清醒期分别有着不同的脑网络状态基础。因此这个转换概率图也定义了进入非快速动眼睡眠,以及从非快速动眼睡眠醒来全脑网络状态的转换。
通过对各个PSG睡眠分期的各个HMM状态的转换次数以及独特状态的范围分析,作者发现这些数值在清醒期要明显大于N2/N3期。更高级和更复杂的状态组成对于支持清醒时的意识非常重要,这个观点已经被很多TMS和EEG研究所证实。
图7.d反映了从清醒期到非快速动眼睡眠期的关键轨迹,即从增加的DMN激活开始向非快速动眼睡眠过渡(先到N1,再到N2、N3)。DMN与内向的心理状态有关,因此作者的结果可能提示DMN是睡眠初始的‘门’。睡眠初始阶段的全脑网络分析对于理解类似失眠和过度嗜睡有很大帮助,因为PSG标准很难适用于这些疾病。有研究表明N2睡眠的转换不稳定,伴随着到达N3困难是失眠的一个重要特质。在转换图中作者可以发现N2-以及N3-相关的全脑网络状态形成一个强的三角回路(图7.e)。这种稳定的转换结构可能在失眠患者身上缺乏。
HMM和PSG的两个主要不一致时N1睡眠期和WASO(睡后清醒期)。N1睡眠期跟任何一个单一的或者单组的HMM状态都不对应。这可能提示PSG定义的N1期并不是一个有着清晰界限的睡眠期,而是一个理解甚少的混合着清醒和睡眠的时期。后续作者们也提供了很多证据证明N1睡眠期可能不是一个单独的睡眠期。
PSG不能区分睡前以及睡后清醒时人们的脑活动。人们在睡梦中惊醒过来时,往往感觉到摇摇晃晃,行为学研究也表明这个时候人们的认知也下降。有一个术语叫“睡眠惯性“也被用来描述这个现象。作者的研究也表明入睡和清醒这两个是不对称的过程,导致两个分开独立的全脑转换模式,一个是在清醒期,另一个出现在睡眠稳定期后。

图7人类清醒-非快速动眼睡眠循环的全脑网络视图。对结果的主要讨论已经在图中被重点标注。方框内的内容为HMM分析得到的新的见解。
总结:
总体来说,作者的研究表明数据驱动的对时间敏感的大尺度脑活动分析能够被用来探索清醒-非快速动眼睡眠循环的行为和认知的本质变化。作者的结果揭示一个传统睡眠PSG以及严格依赖PSG的神经影像研究所有不能提供的高度复杂的脑活动现象(在清醒-非快速动眼睡眠循环期间)。
作者将传统的睡眠分期投射到全脑网络状态的概率转换图上。通过研究这些概率转换图,作者发现在非快速动眼睡眠的稳定阶段,全脑动态性明显减低(HMM状态转换次数少、独特的HMM状态也少)、睡前与睡后的脑活动明显不同、全脑网络活动不支持N1睡眠的传统定义标准,以及DMN活动增加可能是进入非快速动眼睡眠的大门。未来的研究可以使用其它模态,比如MEG和高密度EEG来探索快速动眼睡眠、睡眠疾病、麻醉以及迷幻体验。
原文:
Discovery of key whole-brain transitions and dynamics
during human wakefulness and non-REM sleep
ABA Stevner, D Vidaurre, J Cabral, K Rapuano… - Nature …, 2019 - nature.com

微信扫码或者长按选择识别关注思影
第十四届磁共振脑网络数据处理班(重庆,7.26-31)
第三十届磁共振脑影像基础班(南京,7.31-8.5)
第十届脑影像机器学习班(南京,6.30-7.5)
第十二届磁共振弥散张量成像数据处理班(南京,6.18-23)
第二十届脑电数据处理中级班(重庆,8.9-14)
如对思影课程感兴趣也可微信号siyingyxf或18983979082咨询。觉得有帮助,给个转发,或许身边的朋友正需要。请直接点击下文文字即可浏览思影科技其他课程及数据处理服务,欢迎报名与咨询,目前全部课程均开放报名,报名后我们会第一时间联系,并保留名额。
小动物磁共振脑影像数据处理班(预报名,南京)
第二十一届脑电数据处理中级班(南京,9.7-12)
第七届眼动数据处理班(南京,7.26-30)
脑电信号数据处理提高班(预报名)
脑磁图(MEG)数据处理学习班(预报名)
思影科技功能磁共振(fMRI)数据处理业务
思影科技弥散加权成像(DWI/dMRI)数据处理
思影科技脑结构磁共振成像数据处理业务(T1)
思影数据处理业务三:ASL数据处理
思影科技脑电机器学习数据处理业务
思影数据处理服务五:近红外脑功能数据处理
思影数据处理服务六:脑磁图(MEG)数据处理
招聘:脑影像数据处理工程师(重庆&南京)
BIOSEMI脑电系统介绍
目镜式功能磁共振刺激系统介绍