慢性抽动障碍(chronic Tic Disorder,cTD)和Gilles de la Tourette综合征(GTS,抽动秽语综合征)是由于运动和非运动皮层-纹状体-丘脑-皮质(motor and non - motor cortico - striatal - thalamo – cortical,CSTC)回路功能障碍导致的抽动释放和伴发疾病。与边缘、边缘旁和CSTC网络有联系的前额顶叶网络(Fronto - Parietal Network,FPN)连通性受损被认为是抽动障碍发病的一个原因。本研究探索cTD和GTS中FPN功能连接受损程度在抽动障碍严重程度和伴发疾病严重程度中的作用。通过记录cTD和GTS病人静息状态下脑电、分析eLORETA电流源密度,计算滞后相位同步(Lagged Phase Synchronization,LPS)来估计皮层区域之间的非线性功能连接。结果表明,FPN的连接异常可能与GTS及其伴发疾病的严重程度有关,而感觉运动区的连接异常可能与GTS和cTD的抽动严重程度有关,FPN和感觉运动区的异常连接是影响抽动障碍和相关伴发疾病严重程度和发病频率的原因,且两组病人的脑功能连接紊乱在特定频段上有所不同。本文发表在Progress in Neurobiology杂志。
1.前言
抽动障碍是一种突然发生的快速、反复、无节律、类似痉挛的运动障碍,涉及一个或多个肌肉或发声,常伴有前兆性冲动。抽动障碍(Tic disorder,TD)可以是简单的,也可以是复杂的,这取决于主要的运动特征;此外,抽动障碍可以分为临时性TD(provisional TD,pTD,以前称为短暂性TD)、慢性(持续性)TD(cTD)和Gilles de la Tourette综合征(GTS)。
简单TD通常涉及孤立肌肉群或单一解剖区域,而复杂TD(行为类似于目标导向的但是并没有明显目的)涉及多个肌肉群。此外,TD还必须根据是否存在声音抽动、持续时间、发病年龄以及是否存在任何其他潜在原因(包括医学治疗和药物/物质滥用)进行特征描述。此外,抽动可以是阵挛性或非张力性的(即持续时间较长并导致持续的异常姿势或运动)。
pTD主要特征是出现简单运动性抽动的时间短于一年,否则应诊断为cTD。后者的特点是短暂的,不可控制的,痉挛样动作或声音爆发(语音抽动),且两者不能同时存在。如果同时存在身体抽动和声音爆发,则可诊断为GTS。GTS特征是有多个运动性抽动(包括眨眼、摇头、触摸或嗅物体、重复观察到的动作)和一个或多个声音抽动(突然、短暂、间歇的简单声音,包括呼噜声和清嗓声,或复杂的发声,例如:重复别人的话或短语)。GTS症状出现在儿童期,持续至少一年且中间缓解期不超过三个月。通常,运动性抽动先于发声抽动。此外,病人身体有不舒服的感觉,如瘙痒、刺痛或紧张(即前兆性冲动),而抽动可以缓解这种感觉。这些症状可能会严重干扰交流、日常运作(例如,“阻塞性”抽动)和生活质量。最后,一些其他认知或行为障碍可伴随抽动症状而生,即伴发疾病,包括情绪和焦虑障碍、强迫症(Obsessive −Compulsive Disorder,OCD)和注意力缺陷/多动障碍(Attention −Deficit/Hyperactivity Disorder,ADHD)。此外,还应考虑未另行规定的抽动障碍(包括与链球菌感染相关的儿童自身免疫性神经精神障碍,以及包括所有其他急性发作强迫症和/或TD的儿童急性发作神经精神综合征)。
一些药物,包括抗精神病药、ADHD药物、中枢肾上腺素能抑制剂、选择性血清素再摄取抑制剂和抗癫痫药物,可以帮助控制抽动或减少伴发疾病,并且可以通过肉毒杆菌毒素注射和深部脑刺激来控制耐药性形成。所有的药物治疗都必须伴有行为疗法和心理疗法。然而,上述许多药物可能有显著的副作用,也可能对大量病人无效。
TD治疗的一个关键问题是,对该病的病理生理学知识仍然有限。研究表明,抽动障碍与强迫症具有相似的临床现象、伴发疾病和遗传模式。神经生理学和神经影像学数据揭示了抽动障碍与强迫症疾病在遗传(基因)和环境因素共同作用下额叶皮质、辅助运动区(Supplementary Motor Area,SMA)、运动前区、纹状体、苍白球和丘脑之间的网络功能异常。这些异常包括(CSTC,运动和非运动皮层-纹状体-丘脑-皮质)环路内神经递质释放(包括多巴胺和血清素)受损,导致抽动和伴发疾病。特别是,抽动障碍感觉运动网络抑制失灵。颅磁刺激研究表明,GTS、局灶性肌张力障碍和强迫症患者的初级运动区神经元抑制和促进功能异常,且强迫症病人的感觉运动整合过程异常。这种感觉运动增强可能是由于于边缘-运动CSTC环路失调,这也解释了包括强迫症在内的许多伴发疾病。此外,由于CSTC网络受损,额叶区域不能抑制TD病人的抽动发生(感觉门控异常后,在感觉运动区域产生),以及重复的、侵入性和往复性的运动,复杂行为和侵入性思想。尽管如此,额顶神经网络(FPN)损伤对抽动障碍病人认知和运动功能损害程度的作用仍有待阐明。然而,FPN损伤被认为是TD发病的一个因素,并且静息研究也支持该发现。有证据表明,即使在没有抽动表现时TD病人的大脑状态也与健康对照者不同。此外,FPN可能在控制边缘、边缘旁和CSTC(运动和非运动皮层-纹状体-丘脑-皮质)网络中发挥相关作用,这能够解释解释抽动表现和认知-行为伴发疾病。
因此,本研究假设不同程度的FPN连接损伤可能导致不同程度的抽动障碍和认知-运动功能损害,通过记录TD病人静息状态下脑电(EEG)来表征FPN的功能连接。将TD病人的静息状态脑电记录与年龄和性别匹配的健康儿童(HC)进行比较。此外,比较了无抽动的间隔和立即抽动前时期以探索抽动障碍的大脑振荡动力学表征。最后,本文研究了功能连接与症状严重程度之间的关系。
2.材料和方法
2.1.被试
筛选了精神科所有GTS或cTD儿童,以便纳入研究。对病人进行至少一个月的随访,以监测TD特征。采用了以下纳入标准:(i)符合DSM−V标准的TD诊断;和(ii)频繁(每小时一次)抽动和/或存在发声抽动。癫痫发作病人、服用显著改变皮层兴奋性药物(用于伴发疾病病人的除外)以及头部或颈部抽动导致头部过度运动的病人除外。因此,13例GTS病人和11例cTD病人被纳入本研究。表1总结了病人的人口统计学和临床特征。15名年龄和性别匹配的HC作为对照组纳入研究。
2.2.临床评估
抽动障碍严重程度采用耶鲁大学全球抽动障碍严重程度量表(YGTSS)和DSM−5(SCID−5−RV)结构化临床访谈的研究版本来测量。临床医生评级的半结构化访谈YGTSS用于量化抽动。它提供了运动和发声抽动分数与他们的总体损伤和整体严重程度评分。具体而言,按50分制进行评级,由0(无)和50(严重)构成。整体严重程度评分是运动抽动总分、发声抽动总分和总损伤等级(范围0-100)的总和。
2.3.脑电图记录和预处理
用19导脑电设备进行脑电图记录。根据国际10-20系统放置电极。EEG数据以512Hz的频率采样,做0.3–70Hz(50Hz陷波)滤波,参考电极设在双侧乳突。电极阻抗始终保持在5kΩ以下。根据受试者的耐受性(平均33±7分钟),尽可能长时间记录睁眼/闭眼静息数据。通过排除(通过视觉检查)眨眼、肌电和心电伪迹以及有睡意的脑电周期,离线去除EEG伪迹。之后通过ICA人工去除成分。
无伪迹EEG被分割为2秒的时间段(平均获得748±166个周期),并进行eLORETA分析,以估计七个频段的电流源密度的皮层分布:δ(2–4 Hz),θ(4–8Hz)、α1(8–10Hz)、α2(10–13Hz)、β1(13–20Hz)、β2(20–30Hz)和γ(30–70Hz)。首先通过体素定义了感兴趣皮层区域(ROI),该方法基于蒙特利尔神经研究所MNI−152坐标的电极位置对应皮层体素。然后,使用LPS(滞后相位同步)来估计ROI的非线性功能连接。
2.4.时频功率和连通性分析
使用EEGLAB默认的Morlet小波变换和短期傅立叶变换计算事件相关频谱扰动(Event −Related Spectral Perturbation,ERSP)。原始脑电记录用抽动发作(抽动频段1.2±0.2/min,范围0.5−2)标记,然后用ICA分析以识别非伪迹成分,其持续激活时间为抽动发作标记的-4-10s(平均获得40±10个时间段)。使用随分段频率线性增长的循环次数(3-15)和3.3s的滑动窗口对1到70Hz的信号进行时频分析,以生成-2.3-2.3s 时频数据(12毫秒步长)。将单次试验值平均并转换为db单位。将-1-0s的平均功率设为基线。然后对独立成分进行eLORETA分析。使用体素定义的ROI计算LPS,以评估抽动期间ICA解析源的动态连通性。
2.5.统计分析
eLORETA电流源密度的分析采用:
(i)非参数统计映射方法(Statistical nonparametric Mapping SnPM),包括由对数转换的电流源密度功率在各频段上的体素-体素的独立F检验的组间差异;
(ii)皮层体素差异的非参数置换检验(阈值为5%)。
使用独立样本t检验(19个ROI=171个连接×7个频段=1197次检验)比较各组之间每个频段的ERSP和ROI-LPSs值。基于最大统计量的eLORETA非参数置换被用于多重比较。使用皮尔逊或点-双列相关检验对临床和电生理数据进行相关分析。
3.结果
cTD和GTS病人的人口学特征和YGTS评分无显著差异(表1)。与YGTSS量表一致,所有患者均至少有多种离散的抽动障碍。
3.1.HC(健康被试)与病人绝对平均功率的源分析
图1显示了HC和病人之间eLORETA电流密度值的显著差异。一般来说,HC在δ、α1、β1、β2和γ频段的eLORETA电流密度值高于病人,而病人在θ和α2频段的eLORETA电流密度值高于HC。其中,额叶上回(BA10)的δ和β1、枕中回(BA19)的θ和γ、楔前(BA7)的α1、中央后回(BA3)的β2、额叶上回的γ这些频段上,HC的eLORETA电流密度值显著高于病人。相反,病人eLORETA电流密度值在楔前的δ、额叶上回的θ、α1和β2、中央前回(BA4)的α2、额叶内侧回(BA8)的β1、中央后回的γ频段显著高于HC。
HC在中央后回(α2和β2)、楔状体(BA18,β1)和颞上回(BA39,β1)、额叶内侧回(α2和γ)以及楔前叶(θ)也显示出高于病人的eLORETA电流密度值。相反,病人在中央前回(α2)和额叶上回(δ−β2)的值高于HC。但这些差异均无统计意义。

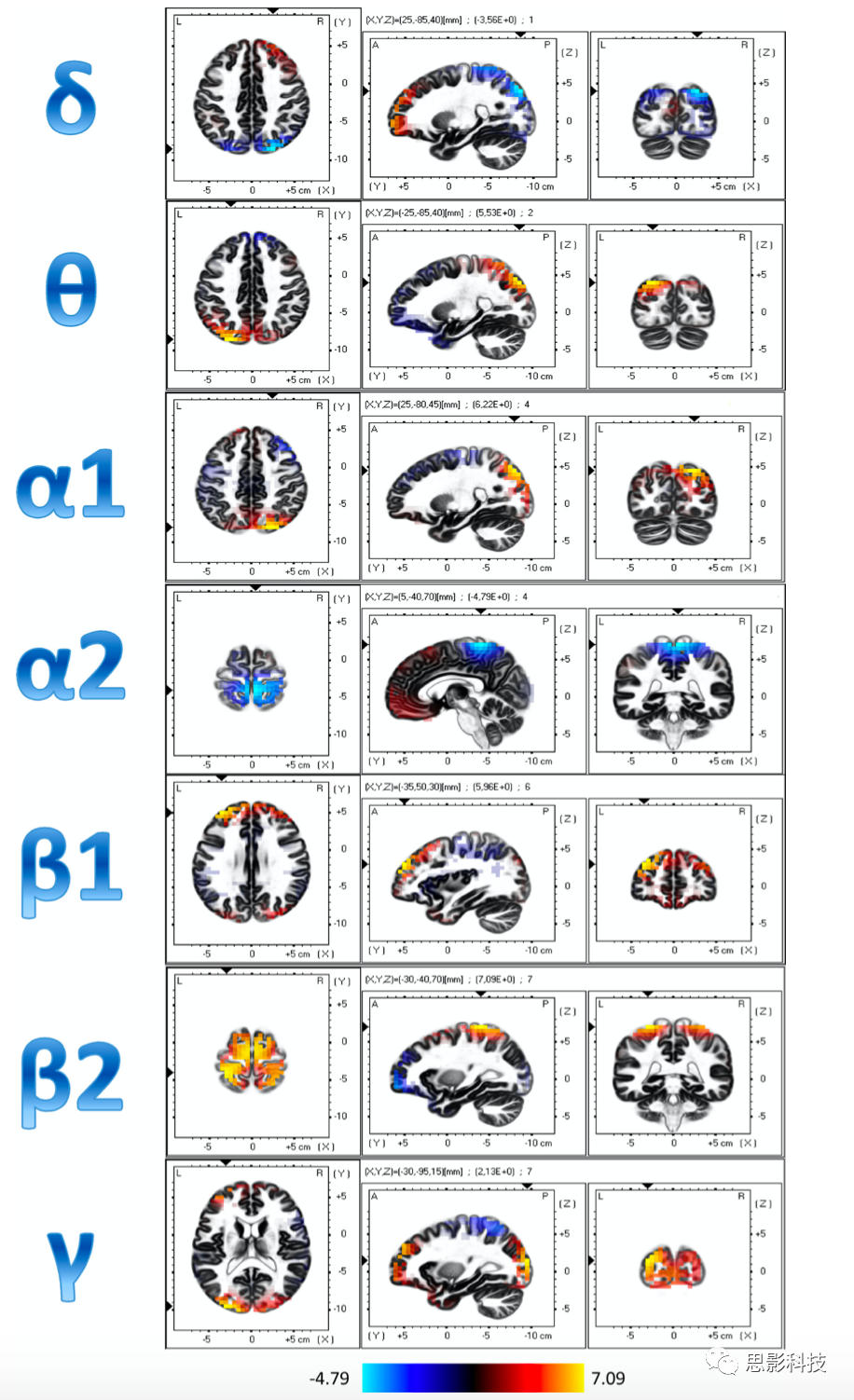
图1。每个频段-体素eLORETA电流密度差值(HC组平均值减去TD组平均值)。红色表示HC中的电流源密度高于TD,蓝色则相反。
3.2.HC与病人的网络差异
功能连通性分析(图2)显示,HC在额顶区的δ和β1、额中央的θ以及顶叶中心区域的β2和γ频段,LPS值比病人更高。相反,病人额顶区的δ,θ,α1和γ以及顶叶中心区域的β1频段LPS下降比HC更为明显。
3.3.GTS与cTD绝对平均功率的源分析
图3显示GTS病人的δ、α1、α2和β2 频段的eLORETA电流密度值高于cTD病人,而cTD病人的θ、β1和γ频段的 eLORETA电流密度值高于GTS病人。其中,GTS的右背侧扣带回皮质(PCC;BA31R)和左侧中颞区(BA21)在β2频段上,eLORETA电流密度值显著高于cTD。相反, cTD的BA10区在β1频段上,eLORETA电流密度值明显高于GTS。
同时还发现,左眶区δ频段(BA47,GTS较高)、BA10区θ频段(cTD较高)、BA47区α1频段(GTS较高)和BA10区(cTD较高)γ频段也存在组间差异。这些差异均无统计意义。
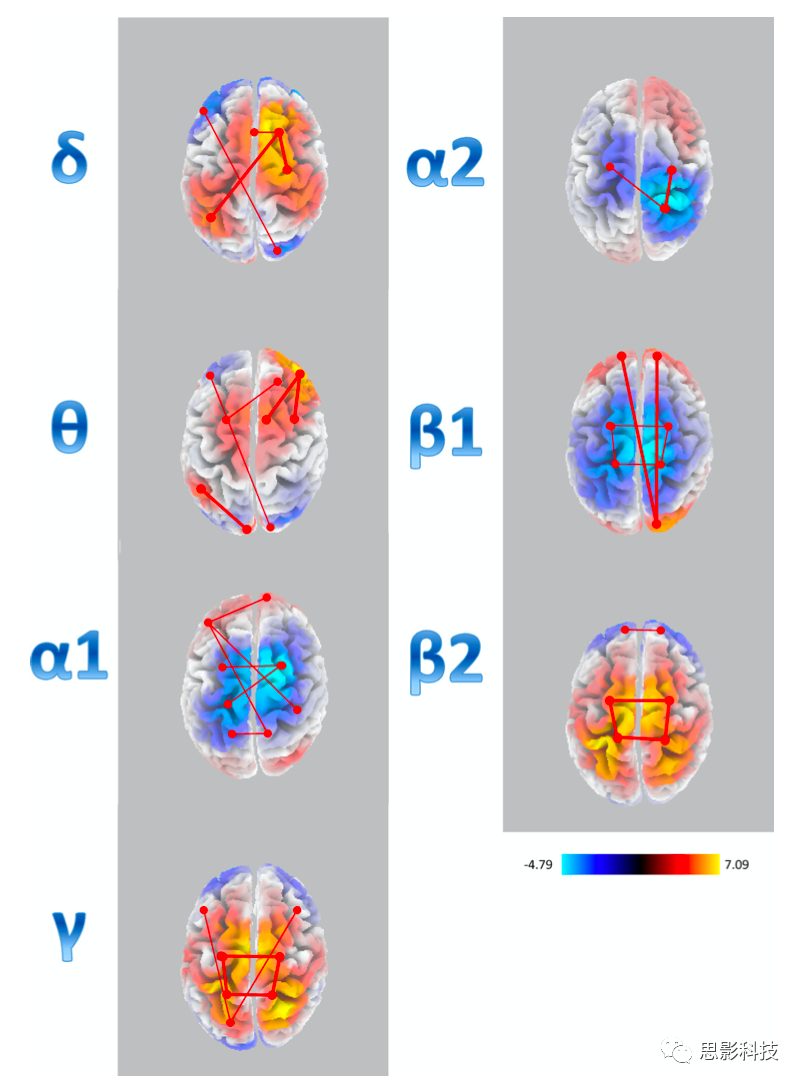
图2。每个频段下LPS值(HC组-病人组的差值)显著增加(粗线)或降低(细线)的功能连通图。

图3。各频段-体素eLORETA电流密度差值(GTS组平均减去cTD组平均)。红色表示GTS中的电流源密度高于cTD,蓝色则相反。
3.4.GTS和cTD的网络差异
与cTD病人相比,GTS病人的功能连接性分析(图4)显示额颞区的δ、颞顶枕区的β2和额叶双极的γ这些频段的LPS(滞后相位同步)更大。相反,与cTD相比,GTS病人额颞和颞-颞的θ和额颞、额枕的β2有更明显LPS降低。在α1、α2和β1频段没有检测到明显的LPS差异(图4)。
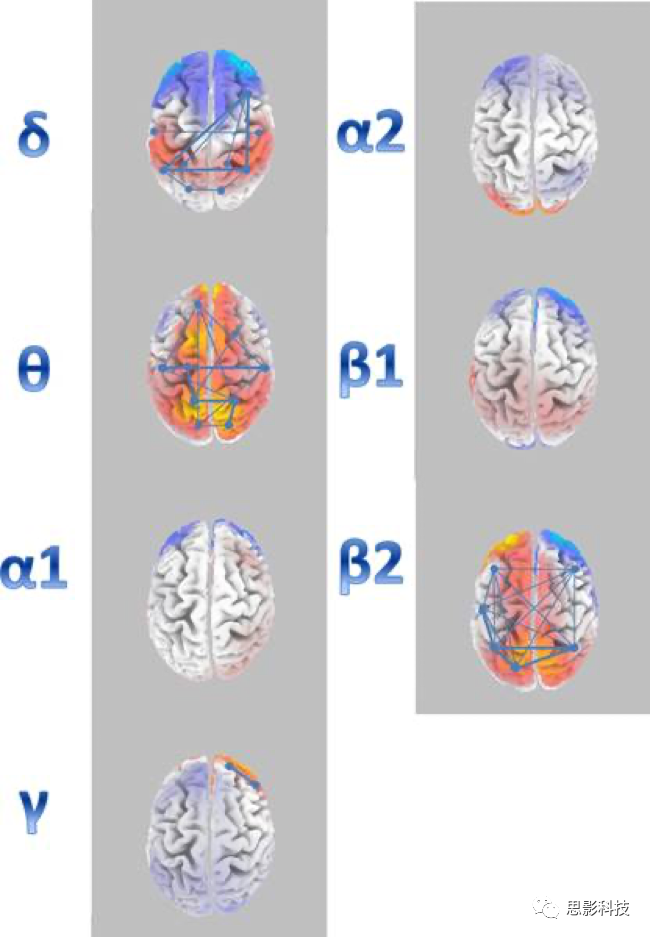
图4。LPS值(GTS组减cTD组)显著增加(粗线)或减少(细线)的功能连通图。
3.5.抽动时的脑振荡活动
ERSP(事件相关频谱扰动)分析显示,两组病人在抽动发作期间感觉运动区均出现双侧的α和β频段失活且无显著差异。相反,与cTD相比,GTS病人在抽动发作前,PCC(BA31)和SMA(BA6)的γ频段激活和β2频段失活,抽动发生后左侧背外侧前额叶皮质(DLPFC;BA9)的γ、β频段激活。cTD在抽动发生后PCC的δ、α1和α2频段失活(图5)。

图5。抽动期脑振荡活动组间差异(GTS组平均减去cTD组平均)。在额叶、运动前区和顶叶区,特别是在后扣带回皮质(PCC)、背外侧前额叶皮质(DLPFC)和辅助运动区(SMA)中,功率有显著差异(白色※表示校正后显著)。
3.6.抽动期间跨ICA解析源的连接动力学
与抽动相关的一些ROI连接无显著性差异,而一些区域表现为连接分析的主节点,包括左侧DLPFC、PCC和SMA(图6)。在重叠边缘的时频点上取GTS-cTD的差值,以确定ROI连通性大小。抽动发作前,GTS病人额叶-枕叶连通性比cTD病人更强,而在抽动后感觉运动区-中央后部区域的连通性也降低的更多。特别地,θ、β2和γ频段的结果表明,GTS病人的DLPFC、SMA和PCC之间具有更强连接,而cTD病人感觉运动区域内α1、α2、β1和β2频段以及SMA-PCC之间的γ频段显示出更强的连接。
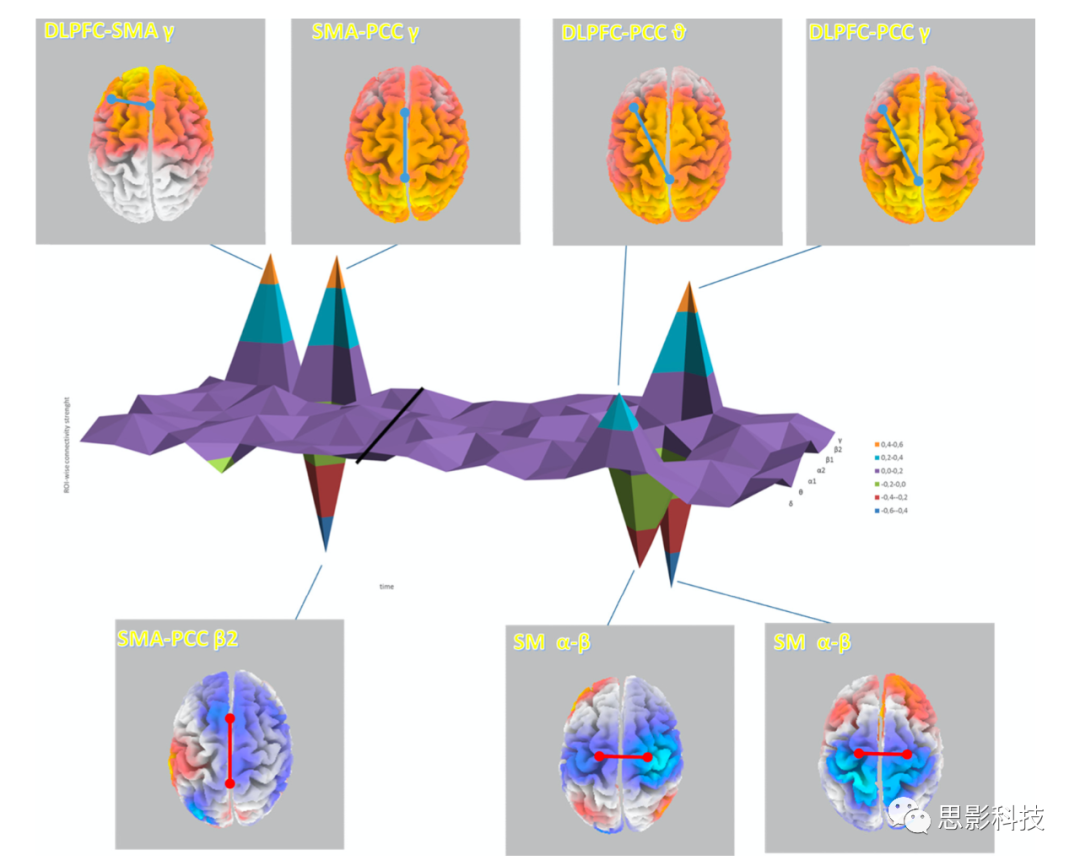
图6。19×19解剖ROI连通性分析结果。突显了组差异显著的频段和ROI(校正后p<0.05)。实心黑线代表抽动发作开始。
3.7.相关性分析
相关性分析显示δ频段在额-顶-颞区域的功能连通性与YGTSS评分呈负相关,即功能连通性越弱(LPS值越低),临床表现越严重(YGTSS评分越高)。此外,还发现β2频段在感觉运动区内的功能连通性与YGTSS呈正相关,即功能连通性越强(LPS值越高),YGTSS的运动成分越严重(得分越高)。另外,TD伴发疾病病人的FPN连接异常程度更高。最后,γ频段在额叶-顶叶-颞区内的功能连通性与前兆性冲动之间存在显著的负相关(图7)。
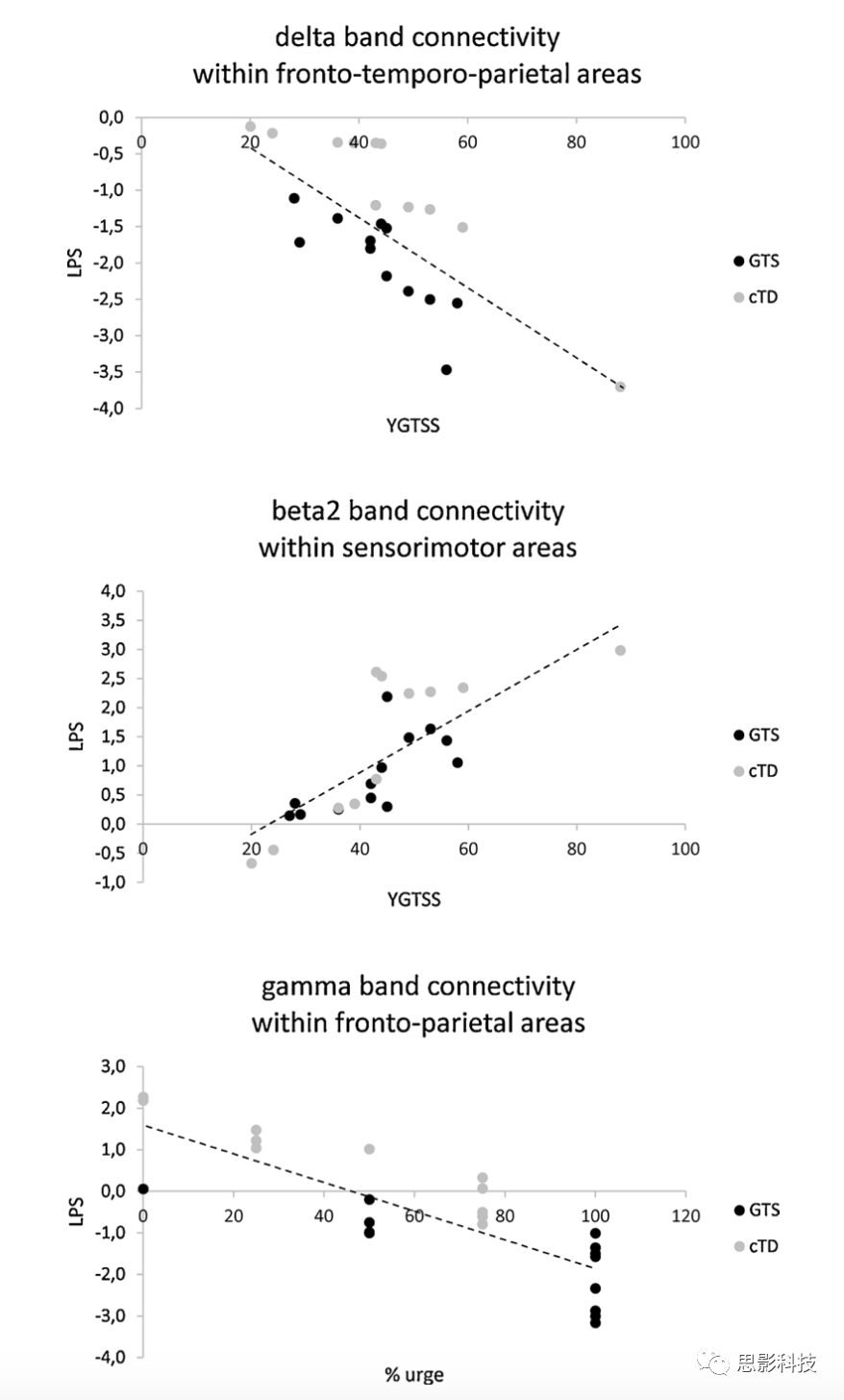
图7。GTS(黑点)和cTD(灰点)病人在不同频段的LPS值与YGTS评分和前兆性冲动百分比显著相关的散点图。
4.讨论
这是第一个针对TD儿童的大范围脑连通性的EEG研究。数据表明,在GTS和cTD中,FPN和感觉运动区的异常连接是导致不同严重程度和发病频率的抽动和相关伴发疾病的原因。而功能连接和神经振荡活动在FPN和感觉运动网络中的特定异常(通过研究源绝对平均功率、抽动期间的脑振荡活动、抽动期间跨源的动态连接并与标准数据进行比较)解释了GTS和cTD之间的特殊差异。
静息态连通性分析显示,与HC相比,病人在δ、β和γ等频段和FPN的特定ROI具有数量不同活跃源,包括DLPFC、SMA、PCC和感觉运动区域。有趣的是,病人在连通性模式上表现出频段特异性的变化,尤其是δ、θ、β2和γ频段在额颞区、颞顶枕区和额极区的表现。尽管本研究的连通性范式不允许区分皮层信息流,但病人的连通性模式与HC明显不同。病人表现出从额叶区域(包括DLPFC和SMA)到后部区域(包括感觉运动区域和PCC)的单一梯度连通性模式损伤,而HC在上述区域中似乎有α、β和γ频段的双向信息流。
病人不同ROI和频段范围的靶向性同CSTC网络一致。尤其是,由于CSTC输出的反常,病人的α振荡中几乎不受影响,因此可能存在有害的α频段相关门的抑制控制。在这一点上,α调制的缺乏可能是基底神经节到脑皮层的神经递质(多巴胺能和5-羟色胺能)传递恶化导致大脑皮层兴奋性GABA调节损伤所引起的。事实上,基底神经节内恶化的γ波传递被认为是抽动障碍的临床指标。当GTS患者试图抑制抽动时,前额叶和皮质运动区之间的α波相干性会增大,这表明α振荡在抽动病理生理中的重要性。因此,考虑到行为背景,在基底节-小脑-颞叶-皮层系统中,α波无法参与抑制活动(其后果是其他频段振荡异常)是导致TD患者运动学习和运动抑制能力减弱的重要原因。TD患者一旦一旦有了这些现象,就可能迅速而坚定地获得相对自动和非自愿的行为(即抽动)。此外,由α调制能力变差导致的不同频段间调制障碍与病人无法从默认模式网络(Default Mode Network,DMN)活动切换到任务模式活动的现象紧密相关。这可能决定了抽动的产生和持续(其标志是cTD和GTS中感觉运动区域之间β2频段连通性的增强)、抑制抽动的能力、伴发疾病和抽动运动程度(其标志物是GTS中δ频段上FPN连通性减弱,非cTD病人)。
这些发现表明,可能是由CSTC网络受损导致的两组病人的FPN功能减退,进一步导致了GTS患者无法抑制侵入性和重复性运动和想法。然而,其他基底神经节,也许是小脑,也可能导致cTD和GTS患者的特异性连通性差异。这些机制值得通过经颅磁刺激-脑电和功能性神经成像方法进一步研究。抽动期间YGTSS和脑振荡活动的相关性以及伴发疾病的存在表明,FPN连接受损程度与抽动严重程度、较强的前兆性冲动和情感调节障碍有关。因此,抽动障碍病人运动抽动症状程度取决于感觉运动区运动输出损伤的严重程度,这与感觉运动区内异常β频段同步呈现出相关性,而CSTC环路的损坏导致了异常运动输出(异常β同步)。事实上,CSTC网络对β振荡产生和运动控制起了很大的作用。此外,β频段连通性受损可能与感觉门控减少有关,后者与皮层运动抑制现象减少所引起的高皮层兴奋性相关,表现为α波无法参与抑制活动,并且可能与CSTC受损有关。
FPN连通性受损会导致除抽动障碍外的伴发疾病。鉴于纯(简单)GTS并不常见,伴发疾病的存在说明具有潜在遗传因素。然而,反向伴发疾病(即伴随GTS的强迫症或多动症)也不常见。因此,这种差异有可能因为有特殊的容易受到环境因素的影响的神经生理学机制。其中,包括多巴胺能和γ-氨基丁酸能在内的一些神经递质系统可能存在明显的功能障碍。这两种神经递质的不平衡可能是行为选择(导致抽动表现)和行为异常的原因。然而,尽管这一领域已经有了重大进展,但尚未完全阐明其潜在的神经病理机制和功能障碍的起始部位。无论如何,仔细评估伴发强迫症在临床上是否与原发性强迫症或抽动相关强迫症相似具有病理生理学和治疗意义。
对于前兆性冲动的神经生物学也可以进行类似的推理。事实上,有更高前兆性冲动的病人在FPN的γ振荡受损更明显地出现在抽动发作前,这与前兆性冲动和抽动之间的时间关联一致。这种γ频段受损很可能是前兆性冲动神经生物机制的一种副现象,因为GTS病人抽动发生时异常岛叶输出过度活跃,引起对先兆感觉的意识增强从而导致抽动发作。然而,扣带回皮质和SMA也与冲动和冲动控制有关。可以假设,γ神经传递受损反映了额叶-顶叶运动控制的抑制性不足(由于丘脑去抑制导致的额叶皮质过度活跃)或不同竞争性运动程序之间的转换不足。因此,由CSTC受损引起的期望运动程序(目标定向行为)和习惯(自动反应)之间的差异可能在CSTC网络的关联运动回路中产生必然的激活,从而产生一种冲动。
静息状态功能连通性结果与先前研究发现的GTS和cTD病人异常神经振荡和连通性情况一致。事实上,考虑到额颞叶、颞顶枕和额极区域内的δ、θ、β2和γ频段之间的关系,目前的研究结果指出抽动障碍病理生理的关键特征是脑网络不稳定性。详细地说,在许多ROI对和频段范围上没有明显的组间差异,GTS和cTD拥有相似的与抽动相关的皮质振荡。相反,正常群体的左侧DLPFC、PCC和SMA是分析θ、β2和γ频段的主要节点。具体而言,快速神经振荡发生在抽动发作之前,并且在包括DLPFC和SMA在内的前额中枢区域有前兆性冲动,而在后部区域(PCC和感觉运动区)中,低频信号占主导地位,其反映了抽动发作。这些研究结果与先前有关抽动发生、表达的FPN区域功能相关性的数据一致。此外,与抽动表达有关的θ-γ频段耦合激活与作为TD病理生理特征的丘脑-皮质节律紊乱模型一致。总的来说,这些结果表明在自发性抽动发作过程中,额叶运动区的宽频振荡活动增强。然而,GTS和cTD病人存在各自独特的抽动发作时的连通性动态调节障碍,GTS组的额叶区域和cTD组的后部区域存在抽动表现相关的较强的连通性。GTS额叶连通性受损,很可能是运动执行前感觉加工受到干扰的表现,因为它发生在抽动之前。这一结果表明,抽动的产生可能依赖于前额叶、额叶和中央顶叶区域之间的信号传输。相反,对于cTD病人来说,感觉运动区域内存在与病人的额顶叶连通性受损一致的局部高连通连通性(PCC是一个共同的节点),可能代表着运动执行的病理性增强,因为它跟随着抽动现象。
4.1.优势和局限性
本研究有两个主要新发现。首先,只有GTS病人有明显的抽动症状相关的FPN连通性受损。这可能是TD的病理生理核心。与cTD病人相比,这种差异可能解释了GTS病人有更明显和时间持续性的抽动、更高的复杂抽动发生率以及并存的运动和声音抽动。FPN连接异常可能反映了CSTC环路功能异常导致的从额叶到感觉运动/颞叶区的抑制控制不佳。目前尚不清楚FPN连接异常是CSTC网络恶化的结果,还是只是抽动障碍的主要特征。前额叶激活与抽动严重程度的相关性和背侧前额叶皮质肥大支持第一个猜测。相反,作为FPN功能连接受损的代偿,GTS病人DMN功能连通性增加。事实上,更高的DMN连接性与较低的抽动严重程度相关,因此表明DMN是在FPN连通性失效之后形成的用来执行运动抑制的机制。因此,本研究假设一旦FPN连接失效程度超过某个阈值,就会发生抽动。换言之,当运动表现所涉及区域的额叶区域的抑制性控制不足,使得CSTC网络的运动回路的异常功能变得明显时,就会发生抽动。因此,除了感觉运动和CSTC网络改变外,FPN连接异常可能主要导致了GTS病人的抽动症状,尽管这一说法值得进一步的证实性研究。
第二, FPN连接异常也可能导致GTS病人伴发疾病(ADHD或强迫症)的发生。事实上,伴发疾病的病人表现出最显著的FPN连接异常。考虑到伴发疾病是由于联合和边缘环路CSTC通路异常引起的,上述CSTC连接异常可能解释了GTS病人ADHD或强迫症的发病率。FPN恶化与伴发疾病之间的相关性进一步证实了当FPN连接异常程度超过一定阈值时,伴发疾病发生的假设。换言之,当额叶区域对涉及抽动以外其他表现的区域(例如边缘、感觉和执行区域)的(缺陷)抑制控制使得CSTC网络运动回路异常变得显著时,就会出现这种伴发疾病。然而,FPN连接异常可能导致TD伴发疾病的说法值得进一步研究。
本研究仍有几个不足:
首先,小样本量可能会限制目前研究结果的一般化。然而,GTS和cTD特异的功能连通性模式仍可以作为诊断标志物,并有望在更大的人群中使用相同的方法来进行研究。
第二,采用了一种相对简单的方法(包括采用带有单个电极和传感器位置的半真实头部模型,而不是真实的头部模型)和脑电图记录设置。虽然这些结果的空间分辨率很低,但发现并确定的与抽动现象有关的重要节点区域与以往研究发现的抽动发生和前兆性冲动相关区域基本一致。此外,与其他神经影像学数据相比,脑电的优势在于它能够捕捉抽动的动态变化。不同的是,本研究发现cTD和GTS病人的大脑连通性受损模式不同。
第三,皮层下信号源的作用仍然是值得怀疑的,因为用头皮记录识别大脑深层区域仍在争论之中。虽然可以通过在脑电分析中使用波束形成器的方法来解决。
第四,考虑到在临床上与原发性强迫症或抽动相关强迫症相似的伴发疾病强迫症可能具有病理生理学和治疗意义,因此伴发疾病可能产生的影响值得在较大样本中进行进一步研究,特别是对有或没有伴发疾病的病人进行比较。最后,需要充分理解神经元和行为波动背后的机制以确定两者是独立的还是直接或间接相关的。这可以通过描述振荡和认知-运动表现之间的动态特征来解决(例如,分析试验-试验相关性)。
如需原文及补充材料请加思影科技微信:siyingyxf 或者18983979082(杨晓飞)获取,如对思影课程及服务感兴趣也可加此微信号咨询。觉得对您的研究有帮助,请给个转发,以及右下角点击一下在看,是对思影科技莫大的支持。

微信扫码或者长按选择识别关注思影
非常感谢转发支持与推荐
欢迎浏览思影的数据处理业务及课程介绍。(请直接点击下文文字即可浏览思影科技所有的课程,欢迎添加微信号siyingyxf或18983979082(杨晓飞)进行咨询,所有课程均开放报名,报名后我们会第一时间联系,并保留已报名学员名额):
第十三届磁共振弥散张量成像数据处理班(南京,9.15-20)
第三十二届磁共振脑影像基础班(南京,9.21-26)
第七届小动物磁共振脑影像数据处理班(南京,12.20-25)
第七届脑电信号数据处理提高班(南京,11.18-23)
脑磁图(MEG)数据处理学习班(预报名)
数据处理业务介绍:
思影科技EEG/ERP数据处理业务
思影科技脑电机器学习数据处理业务
招聘及产品:
招聘:脑影像数据处理工程师(重庆&南京)