自闭症(ASD)是一种具有高度异质性的精神疾病,识别神经解剖学的个体差异可以为ASD的诊断和干预提供有用的信息,但是解决这个问题所面临的挑战在于个体差异与其他原因导致的变异混合在一起。本研究利用机器学习中对比学习的方法揭示自闭症(ASD)中神经解剖学变异结构,将ASD特有的神经解剖学变异结构与典型对照组共有的变异结构分开,ASD特有的变异结构与症状的个体差异有关,这种ASD特有的变异结构也解决了关于ASD的一个长期争论,至少在神经解剖学方面,个体不会聚集成不同的亚型;相反,它们是沿着连续的维度组织的,影响着不同的脑区。可结合以下脑影像机器学习相关文章阅读,加深理解,感谢帮转支持(直接点击,即可浏览,加微信号siyingyxf或18983979082获取原文及补充材料):
卷积神经网络
神经影像预测精神疾病及心理健康的前景
用于阿尔茨海默症分期早期检测的多模态深度学习模型
基于磁共振成像的脑龄研究:可解释的人工智能的当前状态和未来挑战
神经影像研究驱动的脑龄估计作为脑疾病和健康状况识别的生物学标记
基于原始影像数据的深度学习模型预测脑龄可获得可靠的遗传生物标志物 AJP:精神分裂症患者大脑加速老化的纵向识别研究 基于全球14468名被试MRI数据特征预测脑龄和疾病的深度学习模型 AJP:有和没有内化性精神障碍的受虐女孩情绪回路延迟成熟的差异性重度抑郁症患者的脑龄
基于深度学习和自闭症脑成像数据库(ABIDE)识别自闭症谱系障碍
Radiology:皮层厚度预测轻度认知障碍转化为帕金森痴呆症
Nature子刊:基于深度学习预测家族性阿尔兹海默症患者临床前功能性脑老化
使用多元表征方法提升对大脑-行为之间关系的机器学习研究的泛化
用于临床心理学和精神病学的机器学习方法
PLOS Biology:重度抑郁症多成像中心的泛化脑网络标志物
Nature
Medicine:持续的实验性和临床性疼痛的神经影像生物深度学习在婴儿大脑的磁共振图像分析中的作用(上)参数选择对脑卒中后失语症预测模型的影响大脑数据分类时意外过拟合的危险
Nature Protocols:为解释神经成像中的机器学习模型
Biological Psychiatry: 基于多模态脑影像的个体指标预测-方法
Biological Psychiatry:自闭症的神经亚型研究进展
NPP:结构MRI数据的生理性别分类显示跨性别者女性的错误分
BRAIN:利用机器学习揭示了两种精神分裂症的神经解剖学亚型
Molecular Psychiatry:静息态fMRI预测青少年认知能力
JAMA Psychiatry:脑影像机器学习预测精神疾病患者社会功能
引言
大脑精神疾病已影响了全世界数百万人群,疾病异质性是认识和研究它们的一个主要难题,即被诊断为同一疾病的个体往往表现出不同的行为症状和遗传变异。作者之前研究了ASD的异质性,这是一种较普遍的神经发育型疾病,其特征是社会互动受损、行为模式受限和沟通存在障碍,ASD患者在行为症状、遗传和神经解剖学等方面存在差异。
对ASD进行更具体的诊断和有针对性的行为干预以了解其神经解剖学的异质性可能是提高患者生活质量的关键,然而研究人员尚未确定与症状相关的神经解剖学变异,以适用于不同的被试群体。
作者假设ASD特异性变异是由大脑变化的其他因素引起的,大脑的差异在于许多与ASD无关的遗传因素和环境因素。来自不同个体的神经解剖学数据也因为方法上的干扰而有所不同,如扫描仪不同和扫描中心之间的差异。ASD特异性变异可能很难在这些不相关的变量中进行识别,并且目前用来解决这些问题的方法仍然不能令人满意。例如匹配ASD和典型控制组(TC)被试理论上是有效的,但它假设需要匹配的条件已知,然而神经解剖学是由许多遗传和环境因素形成的,其中一些因素是未知的,这给匹配带来了困难。
为了更好地描述具有ASD特异性的神经解剖学变异特征,作者使用对比变分自编码器(CVAEs)将其从被试群体常见的变异中分离出来。CVAEs从两个不同的群体中提取样本作为输入,从两个共同的变异中分离出一个群体的变异(见图S1)。作者使用CVAEs将ASD和TC被试“共享”的变异中分离出“具有ASD特异性”的神经解剖学特征(图1A)。首先作者确认ASD特异性特征与临床症状相关,而共享特征与非临床症状相关,并以此来验证这些特征。作者使用零自由度参数推广方法将结果复制到一个独立的数据集,并对ASD特异性特征进行聚类分析,以确定是否有不同的ASD神经解剖学亚型。最后作者利用CVAE的特性来识别ASD种群中系统变化的脑区。
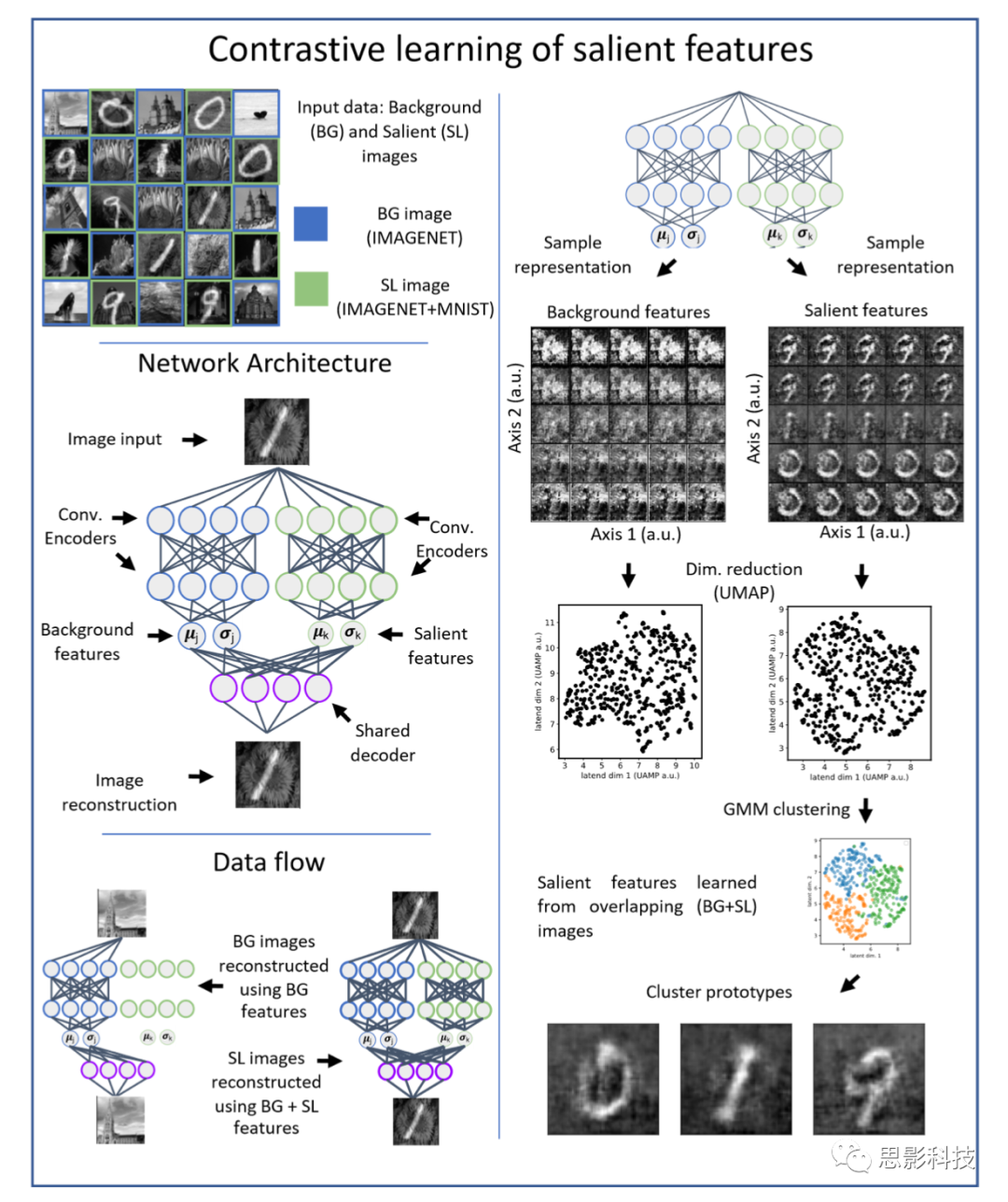
图S1. 使用合成数据演示一个对比变分自动编码器(CVAE)的例子。
合成数据包括背景图像(从ImageNet数据集中选择)和目标图像(将MNIST手写数字数据集叠加到ImageNet图像数据集上创建而成)组成。对比变分自动编码器(CVAE)是一个双流神经网络,用于提取共享的和目标特定特征。背景图像使用共享特征重建,而目标图像利用共享特征和目标特定特征共同创建,因此CVAE学习了不同的共享特征和特定于目标的特征。聚类结果显示,所使用的MNIST数字(0、1和9)由不同的潜在特征表示。
材料与方法
数据集和被试
本研究使用到两个数据集:ABIDE I和SFARI VIP,共计1112名被试,包括539名ASD被试(65名女性)和573名TC(典型控制组)被试(99名女性)。ABIDE I数据集是从17个数据扫描中心收集获得,其中TC组的年龄在6-56岁之间,ASD组的年龄在7-64岁之间。MRI数据集共有341名被试,其中235名被试确认了基因拷贝数变异。两个数据集中被试的年龄分布如图S6所示。
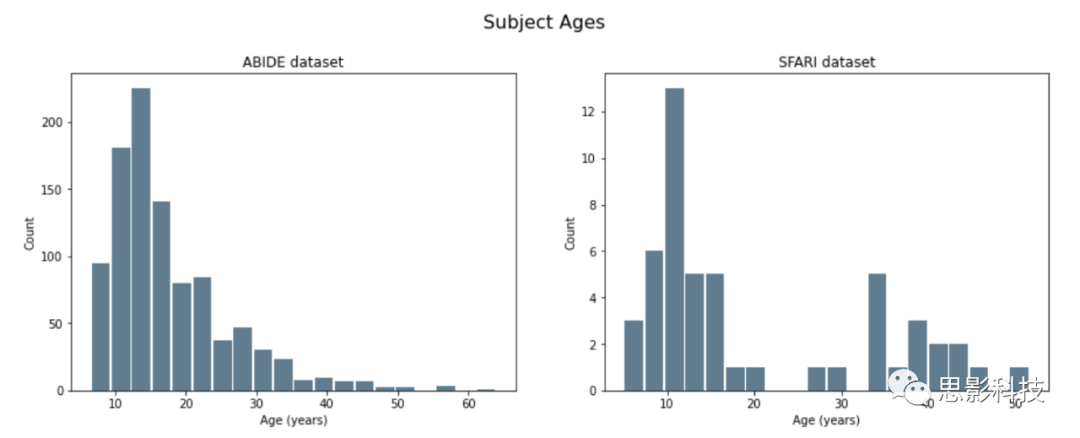
图S6. 两个数据集中被试的年龄分布情况
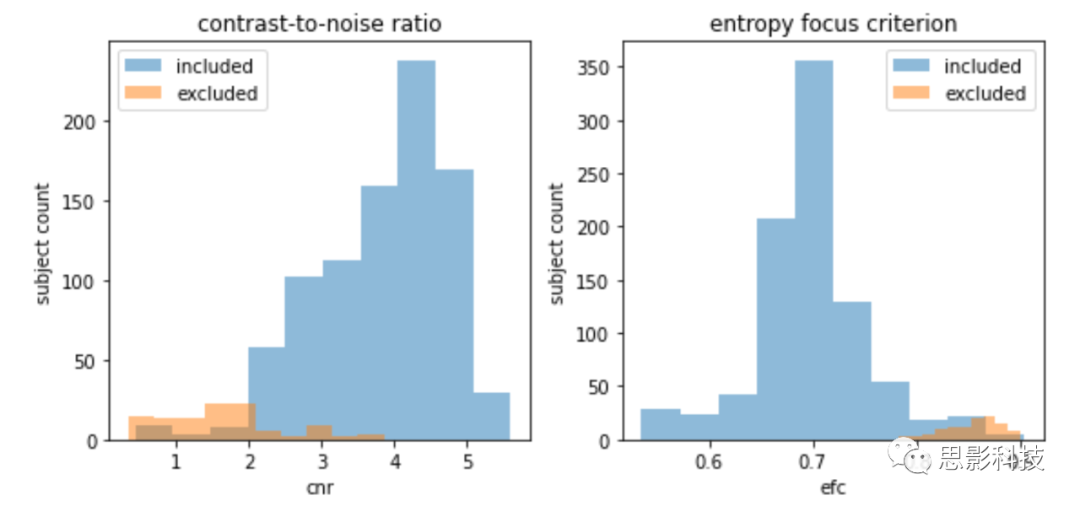
图S7. 解剖扫描的图像质量指标(MRIQC)。109名被排除的被试的组织分割不准确。
MRI数据预处理
ABIDE I数据集中结构像数据包括1099名被试(1112名被试中有13名被试没有结构像数据)。8名被试的数据未能完成分割,109名被试的数据未能准确分割。 SFARI数据集中包含121名被试的结构像和功能像。使用MATLAB中的SPM12工具箱对T1结构像进行预处理,并提取大脑灰质体积和白质体积等特征。
自动编码器的结构
CVAE是基于VAE改进得到,CVAE的输入是大脑体积结构像,分辨率为64×64×64。CVAE由一个编码器和解码器组成,编码器由两个连续卷积层提取共享特征,两个卷积层提取ASD特异性特征(见图S2, 表S1)。编码器将数据分别投影到两个不同的16维潜在分布(共享特征的分布和ASD特异性特征的分布)上。解码器以一个32维的向量(通过串联共享特征和ASD特异性特征获得)作为输入,并产生一个重建的大脑体积结构像作为输出。解码器使用了两个反卷积层,从潜在分布的特征中重建大脑体积结构像。重建后TC(典型控制组)被试的特征维数是32维,由共享特征(一个16维向量)和一个16个零元素组成的向量串联而成。
选择CVAE的原因有以下几点:
首先,CVAEs使对输入特征和潜在特征之间的非线性关系进行建模成为可能,与对比PCA等线性方法相比,CVAE提供了更大的灵活性。
第二,CVAE在其潜在空间中能够分离出共享特征和特异性特征,即使这些特征混合在一起输入,也使得这种方法不同于一些依赖于输入特征的多模态方法。
第三,CVAE包含一个解码器,这使得实现“合成双胞胎”分析成为可能,因为解码器能够根据潜在特征生成违背事实的大脑,从而识别出ASD群体中受到结构变异影响的具有可解释性的大脑区域。
近年来许多新的对比学习方法和多视图学习方法被引入,其中一些方法可能会与CVAE效果相当甚至优于CVAE。例如,在不需要根据潜在特征生成与事实相反数据的情况下,不包含解码器的方法可能会降低计算成本。即使在CVAE中,其他具有更多网络层数的模型也可能表现得更好,特别是在有更大的数据集可用于训练的情况下,探索不同模型的优势是未来工作的一个很有前途的方向。
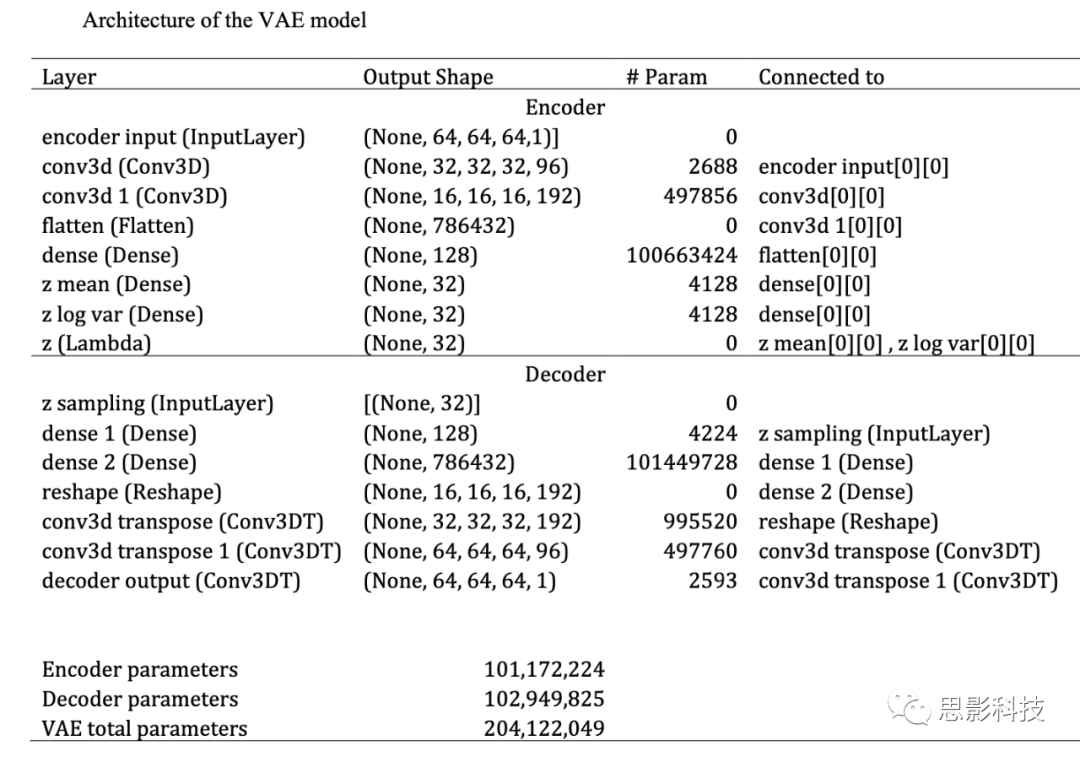
除了CVAE之外,作者还训练了一个标准的变分自编码器(VAE)来进行比较。标准的VAE与CVAE的共享特征的网络分支具有相同的架构,但是它缺少特异性特征的网络分支。为了使两个模型中提取出的潜在特征的维数相等,标准VAE潜在特征的维数与CVAE潜在特征的总维数相同,并且VAE特征维数是CVAE共享特征维数的两倍(表S2)。CVAE和VAE使用ADAM优化器进行训练,当重构误差(输入特征和重构特征之间的均方误差)低于0.005时停止训练。
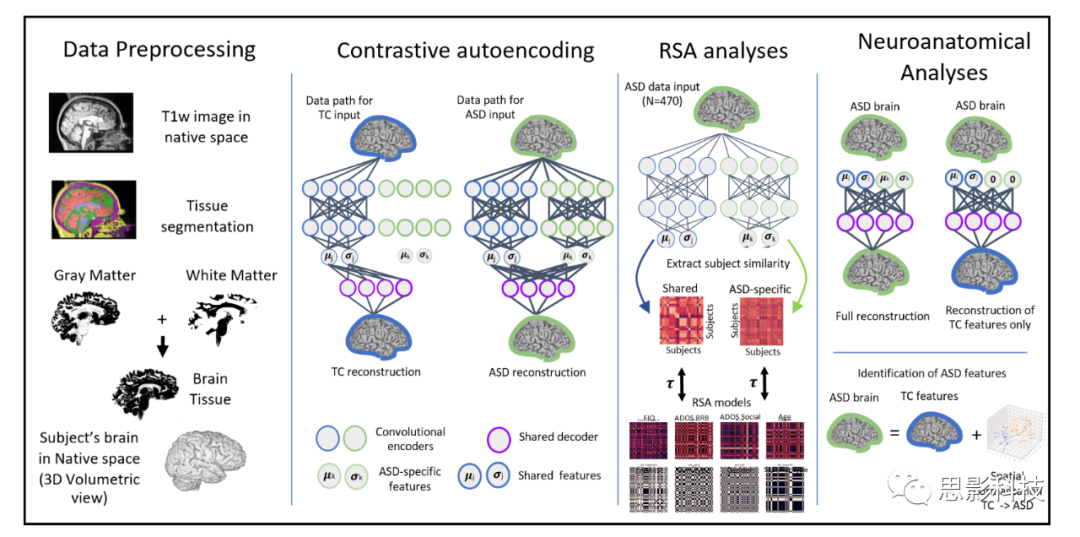
图S2. 研究流程图。
数据预处理:在将数据输入进CVAE前对数据进行预处理。将TC(典型控制组)组(N=470)和ASD组(N=512)被试的T1结构像分割为各个组织,并提取出灰质白质等组织的特征。
对比自编码器:作者训练CVAE,从TC被试共享特征中分离出ASD特异性特征。
RSA(表征相似性)分析:为了探究潜在特征中的信息,作者将共享特征和ASD特异性特征被试之间的相似性与来自行为、人口统计学和遗传数据的相似性模型进行比较。
基于张量的形态学测量:为了识别ASD的神经解剖学相关性,作者使用合成的大脑进行基于纵向张量的形态学测量。对于每个ASD被试,作者使用共享特征和ASD特异性特征或仅使用共享特征来重建他们的大脑体积结构像,然后分析了将TC大脑转化为ASD大脑所需的矢量场的雅可比矩阵行列式。
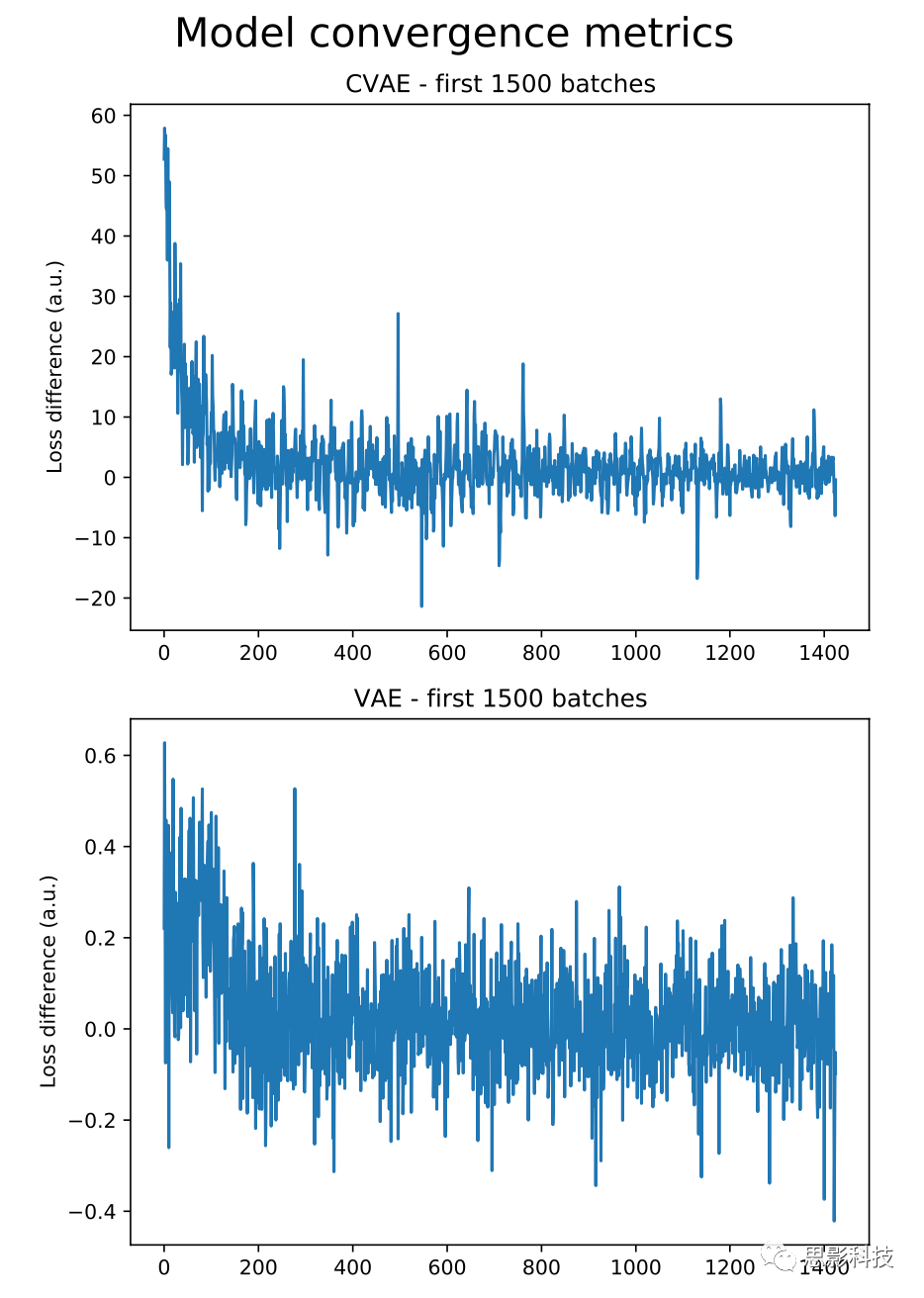
图S3: CVAE和VAE训练集loss的变化情况
表S1. CVAE架构

表S2. VAE架构
请注意,VAE和CVAE都是概率模型。为了估计不确定性,可以从模型中抽取多个样本,并对这些样本进行分析,测量结果之间的方差。
由于深度学习模型拥有大量超参数,因此特别容易出现参数选择不规范的情况。并且在训练集的上表现良好的模型在一个全新的数据集中可能会表现不佳,即泛化性能不佳。在本研究中,作者使用SFARI VIP数据集测试模型的鲁棒性和泛化性能。
如您对脑影像机器学习等数据处理如脑功能,脑网络或其他模态脑影像数据处理感兴趣,请浏览思影以下链接(直接点击即可浏览),感谢转发支持。(可添加微信号siyingyxf或18983979082咨询):
上海:
第二十一届磁共振脑影像结构班(上海,9.19-24)
第二十四届脑影像机器学习班(上海,10.9-14)
第三十一届磁共振脑网络数据处理班(上海,10.28-11.2)
南京:
第六十七届磁共振脑影像基础班(南京,9.15-20)
第五届弥散磁共振成像提高班(南京,9.22-27)
第三十三届磁共振脑网络数据处理班(南京,10.16-21)
第二十二届磁共振脑影像结构班(南京,10.24-29)
北京:
第六十八届磁共振脑影像基础班(北京,9.21-26)
第十届脑网络数据处理提高班(北京,10.20-25)
第十一届磁共振ASL(动脉自旋标记)数据处理班(北京,11.3-6)
重庆:
第九届脑网络数据处理提高班(重庆,10.13-18)
第七十届磁共振脑影像基础班(重庆,10.22-27)
第二十八届弥散成像数据处理班(重庆,11.5-10)
数据处理业务介绍:
思影科技功能磁共振(fMRI)数据处理业务
思影科技弥散加权成像(DWI/dMRI)数据处理
思影科技脑结构磁共振成像数据处理业务(T1)
思影科技定量磁敏感(QSM)数据处理业务
思影科技啮齿类动物(大小鼠)神经影像数据处理业务
思影科技灵长类动物fMRI分析业务
思影数据处理业务三:ASL数据处理
思影科技脑影像机器学习数据处理业务介绍
思影科技微生物菌群分析业务
招聘及产品:
思影科技招聘数据处理工程师 (上海,北京,南京)
BIOSEMI脑电系统介绍
目镜式功能磁共振刺激系统介绍
基于症状、人口统计学特征和扫描部位解剖学相似性比较
在CVAE训练过程中,作者使用一种受表征相似性分析(RSA)启发的方法来探究潜在特征。作者根据不同的人口统计学变量和个体行为学指标计算被试之间的相似性,对于人口统计学变量,如年龄和全尺度智商(FIQ),被试间距离是它们之间欧氏距离的绝对值(即年龄差异或FIQ得分差异)。对于类别变量(如性别或扫描中心,结果为0或1),如果两个被试分类变量之间互相匹配(即拥有相同的性别或相同的扫描地点),被试间的距离为0,否则为1。对于个体行为学属性(如Vineland、WISC和ADOS评分,见图1),作者使用主成分分析(PCA)并计算了第一个主成分负荷的绝对差异。对于ADOS评分,作者包括了总分,以及从单个ADOS中计算出的第一个主成分。为了构建RSA模型,作者使用了来自所有该属性上有评分的被试的数据(例如ADOS总评分,Vineland,见表S3)。
表S3. RSA分析补充材料

为了保证从CVAE的潜在分布中提取的不同样本RSA的稳定性,作者对每个ASD被试的潜在分布进行了10次采样,从而有效地对10个不同的数据集进行重建,然后评估结果的稳定性,确定基于解剖学特征的表征差异矩阵(RDMs)与年龄、性别、症状和遗传等属性的RDM之间的相关性是否大于零(使用单样本t检验)。此外,作者使用配对样本t检验来确定被试属性(即年龄、症状)的RDM是否与基于ASD特异性特征的RDM或基于共享特征的RDM相关性高。
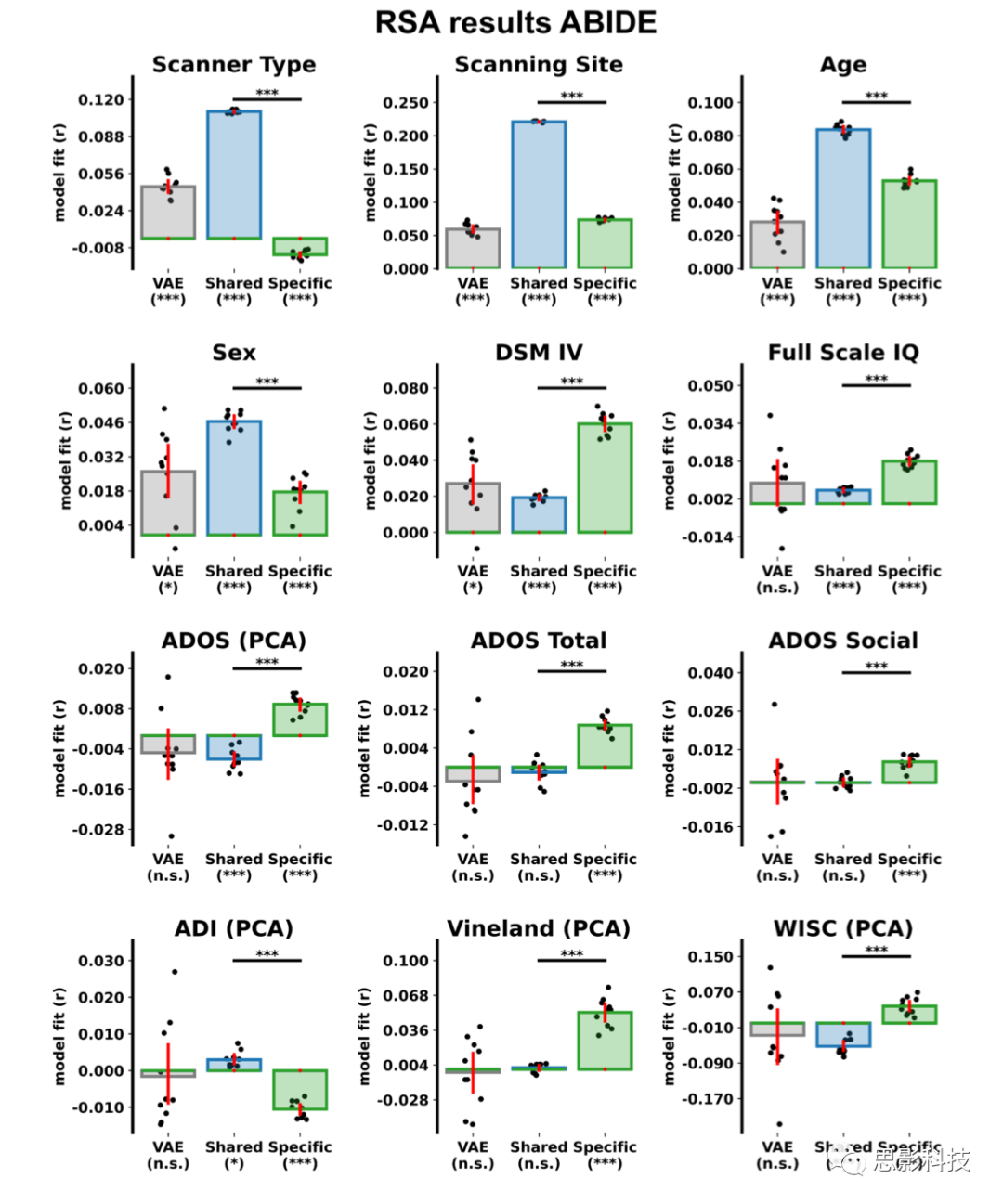
图S4:RSA分析结果(ABIDE数据集)。柱状图显示了神经解剖学特征(VAE、CVAE共享和CVAE ASD特异性)和患者属性之间的表征相似性。五角星表示的显著性(*p<.05,***p<.0001)
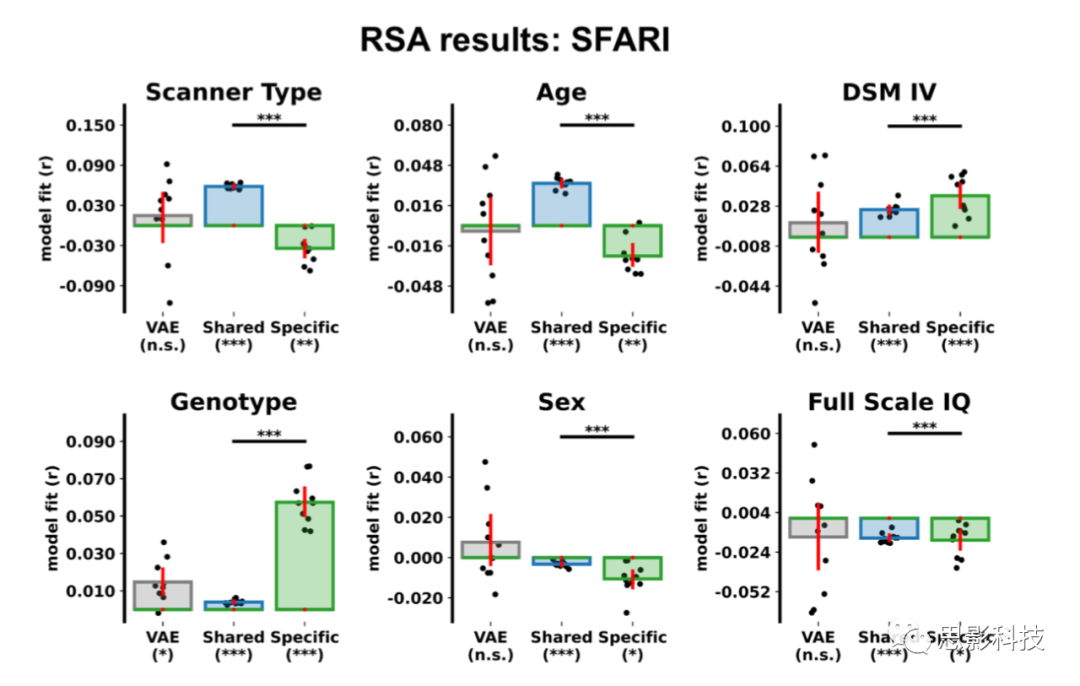
图S5:表征相似性分析(RSA)结果(SFARI数据集)。柱状图显示了神经解剖学特征(VAE、CVAE共享和CVAE)和患者属性之间的表征相似性。(* p < .05, ** p < .001, *** p < .0001).
聚类分析
作者使用肘部法寻找共享特征、ASD特异性特征和VAE特征的最优聚类个数。首先将ABIDE和SFARI数据混合起来,对于这三组特征中的每一组各拟合了一个高斯混合模型。作者使用贝叶斯信息准则(BIC)来衡量聚类个数是否最优。为了确保结果的稳定性,作者对来自(C)VAEs的100个不同的样本重复了这个过程。
与事实相反大脑的合成
为了在神经解剖学中定位到ASD特异性个体差异,作者为每个ASD被试生成了一个病例对照大脑(合成的“TC双胞胎”)。为了实现这一点作者使用CVAE,具体来说,每个ASD输入特征都被映射到共享特征和ASD特异性特征上,同时使用共享特征和ASD特异性特征可以重建为ASD大脑。得到的TC双胞胎大脑具有与ASD输入的相同的共享特征,但没有ASD特异性特征。该方法提高了对传统的病例组-对照组分析的敏感性,类似的方法已被用于图像去噪等领域。
基于张量的形态学测量
在得到合成的“TC双胞胎”大脑后,作者计算了合成TC双胞胎大脑转化为相应ASD大脑重建的变形场,这些变形场揭示了被试特定的与ASD相关的神经解剖学的差异。为了实现这一点,作者使用了非线性扭曲方法将每个合成的TC双胞胎大脑转换为相应的ASD大脑,通过将TC双胞胎大脑转化为重建的ASD大脑并确保5-6张图像都是CVAE的输出,因此它们之间唯一的区别是是否存在ASD特异性特征。
然后作者计算了变换矩阵的雅可比行列式,为了实现跨被试之间的比较,作者将雅可比矩阵映射标准化到一个公共的MNI空间。具体来说,作者估计了一个非线性变换来转换每个被试的解剖学图像以匹配MNI模板,然后将这些变化通过该被试的雅可比行列式图体现。通过计算原生空间中的雅可比行列式对图像进行归一化,避免了将TC双胞胎大脑和ASD大脑分别归一化可能引入的潜在差异。为了识别ASD中个体变异的位点,作者计算了前两个主成分(PC),因为这两个主成分占据了雅可比行列式图中的大多数变异。为了识别与每个PC相关的区域,作者将PC负荷与大脑模板中每个体素的雅可比矩阵行列式值相关联。作者使用了哈佛-牛津解剖图谱(图2)和Neurosynth (图S9)为大脑区域分配标签,并且为了研究两种PC之间的关系和个体差异的关系,作者分别将PC负荷与被试的ADOS得分、年龄和性别相关联。为了保持一致性考虑到一些变量,如ADOS评分是离散的,作者在所有分析中都使用了肯德尔相关性τ。

图S9. 与第二个主成分(PC2)相关的神经解剖学扩张/收缩的区域。黑色轮廓显示了Neurosynth.org自动分析搜索词语“社会”后显著的(z>3.1)区域。
结果
ASD特异性神经解剖学与临床变异有关
作者使用ABIDE I数据集中的fMRI图像分别训练一个CVAE和一个非对比VAE,使用到的数据包括470名ASD被试和512名TC(典型控制组)被试。非对比VAE有一组潜在特征,但在参数数量和潜在特征数量上与CVAE匹配。非对比VAE允许测试神经解剖学和ASD症状之间的关联是否可以单独使用VAE来识别,而不分离ASD特异性和共享变异。
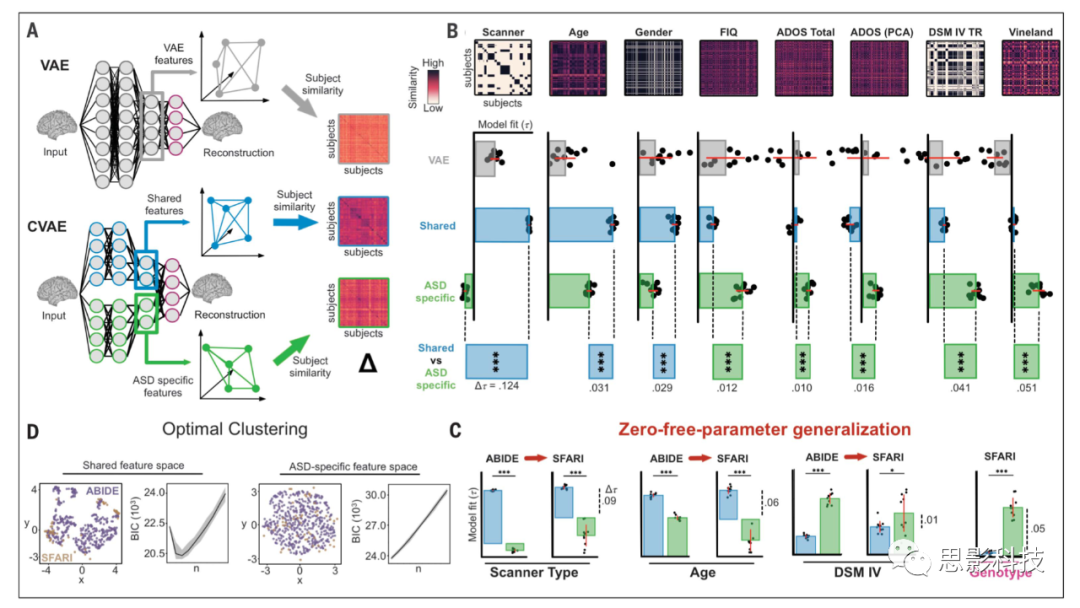
图1. 神经解剖学特征模型。
(A) 从自编码器中提取的神经解剖学特征被用于构建神经解剖学相似度矩阵。
(B) 基于不同被试的属性,将神经解剖学相似度矩阵与相似度矩阵进行了比较。TC和ASD被试共同的变量被共享的CVAE特征捕获,而与ASD相关变异相关的变量被ASD特定的特征捕获。对照模型(VAE)在所有变量中的拟合效果都较差。
(C) 零自由度参数推广。结果推广到一个新的数据集(SFARI),不需要额外的拟合;此外,具有相同拷贝数变异(CNV)的ASD风险增加的被试在ASD特异性方面更相似,但不是共享的神经解剖学特征。
(D) 最优聚类个数。ASD特定特征最优的个体变异由单个聚类簇捕获,而共享特征最优的变异由三个聚类簇捕获。散点图显示了个体被试的神经解剖学数据,从ABIDE(紫色)和SFARI(橙色)数据投影到统一流形近似和投影(UMAP)维度,从共享和ASD特定的特征计算。
作者首先展示了非对比VAE的实验结果,作者使用表征相似性分析(RSA)来检验VAE的神经解剖学特征是否与ASD被试的临床特征和非临床特征相关,如扫描仪类型、年龄、Vineland适应行为量表和自闭症诊断观察量表(ADOS)。作者首先计算了被试之间关于VAE神经解剖学特征之间的两两差异,并得到了一个差异矩阵,然后对每种非临床和临床特征重复这个过程(图1B),最后作者使用肯德尔等级相关系数τ衡量VAE差异矩阵与临床和非临床特征对应的差异矩阵之间的相关性。
实验结果表明VAE提取的神经解剖学特征与一些非临床指标存在肯德尔相关性,如扫描仪类型(τ=0.04, t9=16.29, p<0.001)、年龄(τ=0.03, t9=8.27, p<0.001)和性别(τ=0.03, t9=4.71, p=0.001)。VAE提取的神经解剖学特征与DSM IV亚型之间也存在一定的相关性(τ=0.03, t9=4.77, p=0.001),但与ASD严重程度(ADOS 总分τ=0.00, t9=-1.08, p=0.310)和Vineland量表(τ=0.00, t9=-0.29, p=0.780)不太相关,这与上文提出的假设一致,即VAE特征可能无法捕捉到ASD症状方面的变化。
然后作者评估了用CVAE解开ASD特异性和共享的神经解剖学变异性是否会有助于识别临床相关的个体变异。如CVAE的结构图所示,CVAE将特征分离为ASD特异性特征和共享特征(图1A和图S2),虽然在CVAE训练过程中已隐含地对ASD和TC被试进行二元区分,但该模型没有提供任何有用的临床和非临床个体特征。作者使用RSA比较了CVAE的ASD特异性和共享的神经解剖学特征与每个个体特征的相关性。作者希望发现共享特征与ASD和TC被试共同的非临床变异相关,而ASD特异性特征与ASD临床变异相关(图1B)。
正如预期的那样,扫描仪类型与共享特征中被试之间的相似性相关(τ=0.11, t9=253.01, p<0.001),但与ASD特异性特征无关(τ=-0.01, t9=-14.16, p<0.001;共享与特异性差值:Δτ=0.12, t9=124.83, p<0.001)。因此,CVAE能够排除多中心数据中的变异来源,相比之下,ASD临床症状与ASD特异性特征相关,但与共享特征无关。这些包括与DSM IV的行为亚型的相关性(ASD特异性特征: τ=0.06, t9=30.83, p<0.001; 共享特征: τ=0.02, t9=29.02, p<0.001; 差异: Δτ=0.04, t9=20.04, p<0.001),与ADOS评分的相关性(ASD特异性特征: τ=0.01, t9=16.85, p<0.001; 共享特征: τ=0.00, t9=-1.50, p=0.167; 差异: Δτ=0.01, t9=11.59, p<0.001)和与Vineland适应行为量表的相关性(ASD特异性特征: τ=0.05, t9=12.33, p<0.001; 共享特征: τ=0.00, t9=1.17, p=0.270; 差异: Δτ=0.05, t9=10.46, p<0.001。见图S4)。
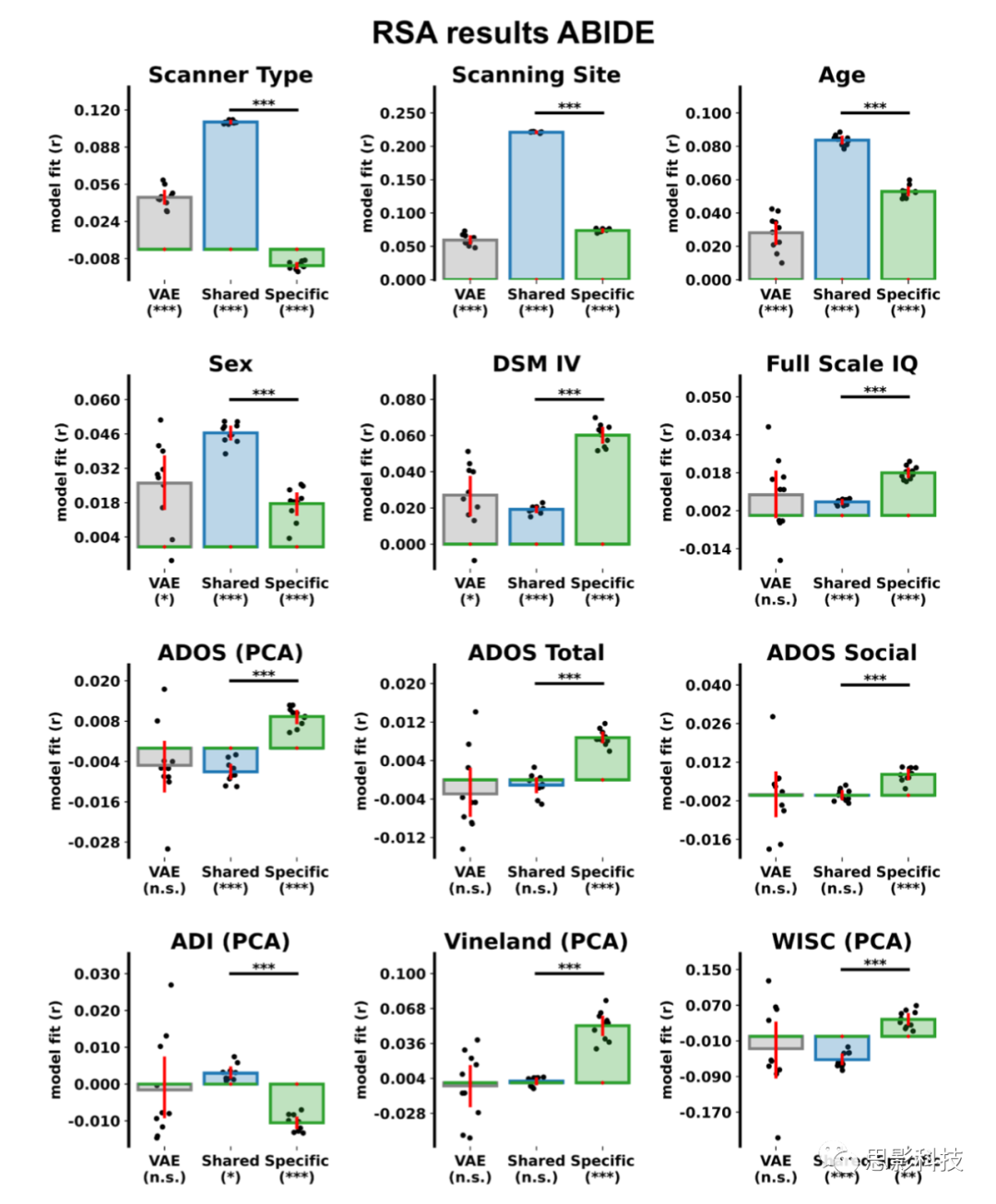
图S4. 表征相似性分析(RSA)结果(ABIDE数据集)。柱状图显示了神经解剖学特征(VAE、CVAE共享和CVAE ASD特异性)和被试属性之间的相似性,星号表示的显著性(*p<.05,***p<.0001)。
年龄、性别和智商(FIQ)的结果比较有趣,因为这些结果已知与TC和ASD被试的神经解剖学有着不同的关系,并且这些属性均与ASD特异性特征显著相关(年龄:τ=0.05, t9=48.60, p<0.001;性别:τ=0.02, t9=8.13, p<0.001;FIQ: τ=0.02, t9=20.22, p<0.001),与共享特征也相关(年龄:τ=0.08, t9=89.29, p<0.001;性别:τ=0.05, t9=35.34, p<0.001;FIQ: τ=0.01, t9=15.57, p<0.001)。这表明CVAE能够将年龄、性别和FIQ的一般作用与ASD特定相互作用分离出来。共享特征比ASD特定特征具有更大的年龄和性别差异(年龄:Δτ=0.03, t9=24.11, p<0.001;性别:Δτ=0.03, t9=24.11, p<0.001),相反,FIQ的变异与ASD特异性特征相关,而不是与共享特征相关(Δτ=0.01, t9=12.86, p<0.001)。
总之,CVAE不仅能够将ASD特有的个体神经解剖学变异性与整个人群特征的变异中分离出来,而且这些变异模式与临床和非临床被试特征存在差异相关。这与对比VAE模型形成对比,在对比VAE模型中,单一的神经解剖学特征与个体特征的相关性较弱。
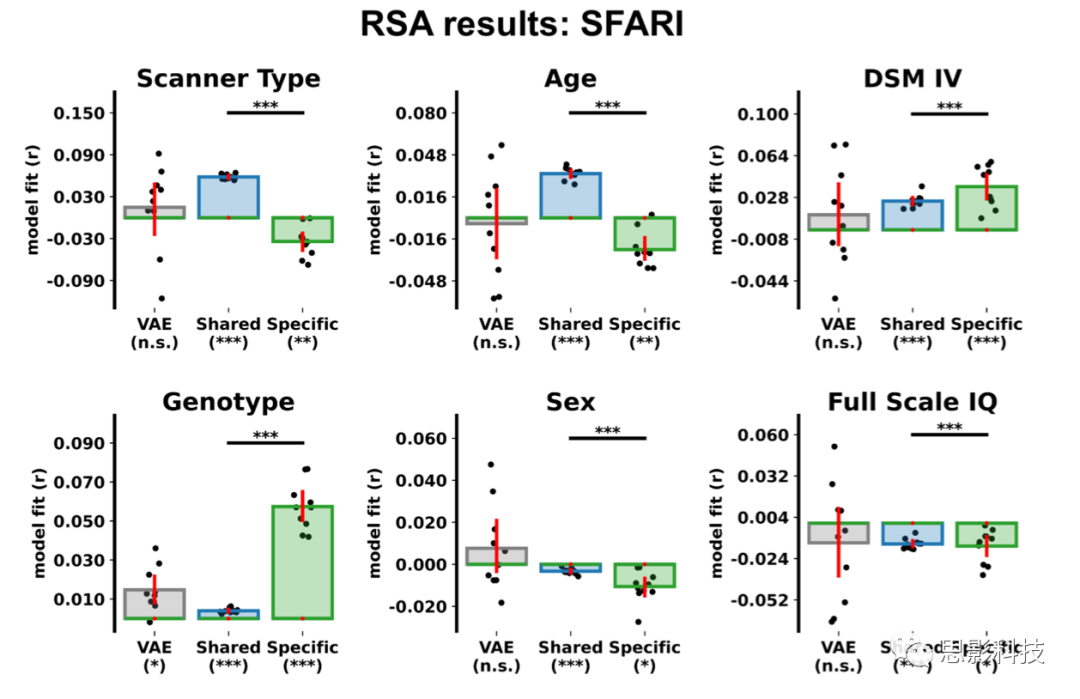
图S5. 表征相似性分析(RSA)结果(SFARI数据集)。柱状图显示了神经解剖学特征(VAE、CVAE共享和CVAE ASD特异性)和患者属性之间的表征相似性。(* p < .05, ** p < .001, *** p < .0001).
独立数据集的推广
对不同数据集的泛化性能被认为是检验模型性能的金标准,所以对跨不同数据集的泛化性能进行检验是有必要的。为了测试模型的泛化性能,作者将训练好的CVAE应用于SEARI VIP数据集(N=121),使用无参数拟合方法进行验证(无须训练或迁移学习),并提供了比交叉验证更严格的泛化性能的测试。
SFARI VIP数据集中包含了ASD相关的拷贝数变异(CNVs)信息,从而能够研究ASD特异性神经解剖学特征是否与基因型相关。作者对SFARI VIP数据集执行与ABIDE数据集相同的特征提取步骤,提取共享特征和ASD特异性特征,比较共享特征和ASD特异性特征的神经解剖学特征相似性与扫描仪类型、年龄、性别、DSM IV亚型和基因型等属性之间的相似性。
作者预计如果CVAE特征是稳定的,那么共享特征应该也与扫描中心、年龄和性别等属性相关,而ASD特异性特征应该与ASD相关的属性相关,如DSM IV亚型。研究结果证实了这些假设(见图S5),即与ASD特异性特征相比,共享特征与扫描中心(Δτ=0.09, t9=12.81, p<0.001)、年龄(Δτ=0.06, t9=15.09, p<0.001)和性别(Δτ=0.01, t9=3.17, p=0.011)的相关性更高。相比之下,ASD特异性特征与DSM IV亚型的相关性更高(Δτ=0.01, t9=2.34, p=0.044),这表明CVAE能够确定群体范围内的神经解剖学模式,其中一些模式被所有被试所共享,而另一些模式只存在于ASD患者中。
此外,在16p11.2缺失和重复携带者中观察到的神经解剖学差异是否与典型发育人群中的变异模式相一致,或者它们是否与ASD中的变异模式相匹配。删除和重复CNVs之间的相似性反映在ASD特异性特征上比反映在共享特征上更好(Δτ=0.05, t9=14.54, p<0.001)。作者注意到与CNVs相关的神经解剖学表型可能只是更广泛的ASD的一个子集:超过200个CNVs与ASD相关。未来发展更大规模的基因分型数据集将对下一步的研究至关重要。
变异的性质
研究人员对ASD的个体差异理解为不同的亚型还是连续维度的变异存在争议,在确定了ASD特异性特征后,使得这些假设得到直接验证成为可能。作者使用高斯混合模型算法对所有被试的潜在特征聚类,并使用贝叶斯信息准则(BIC)来确定最优聚类个数(图1D)。
因为CVAEs和VAEs是概率模型,所以作者确定了100个潜在特征的最优聚类个数。所有被试的VAE特征中100%的样本被分为单个簇(p<0.01;图1D),CVAE的结果更加微妙,对于共享特征,100%的样本被分为多个簇(p<0.01)。然而,基于ASD特异性特征的被试分布再次表明存在连续的变化,100%的样本被分为单个类(p<0.01)。因此,聚类分析的结果表明,一旦从典型的变异中分离出来,与ASD相关的神经解剖学变异可以被连续的维度更好地捕获而不是离散的类别。这一结论适用于这里所考虑的神经解剖学数据,其他数据集(例如fMRI)可能会揭示多个聚类。
神经解剖学解释
为了确定ASD被试神经解剖学变异位点,作者遵循了一个包含三个步骤的方法。首先第一步,对于每个ASD被试,作者只使用共享特征重建他们的大脑,这些特征代表了独立于诊断的个体差异(在使用CVAE解码器之前,作者将ASD特异性特征的值设置为零),得到的结果是一个“合成的TC双胞胎”:一个模拟的大脑与最初的ASD被试相匹配,但是对ASD特异性特征缺乏分析。第二步,作者通过非刚性转换估计了一个与事实相反的TC被试的大脑,以匹配相应的ASD被试的大脑。这也产生了一个向量场,从而描述了ASD大脑和相应的TC大脑之间的差异。第三步,作者计算了向量场的雅可比矩阵行列式。该测量方法捕获了将模拟的TC大脑转化为相应的ASD大脑进行的局部体积压缩和扩张。对所有被试重复此过程后,作者计算了不同ASD被试组中灰质和白质的变化情况。
为了归纳具有可解释性的神经解剖学特征,作者计算了所有ASD被试(N=470)的雅可比矩阵图的前两个主成分(PCs,见图S8)。然后作者通过计算每个体素,测量了每个PC上不同大脑区域的压缩和扩展的系统变化,并且计算了该变化与雅可比行列式之间的相关性(图2,阈值为p<0.05,通过Bonferroni校正)。通过关注表现出最大差异的两个PC,作者注意到虽然在某些区域(如丘脑)的检测强度对比相对比较困难,但这是TC和ASD大脑的共同特征;伴随的变化应该被共享特征所捕获,而不是ASD特异性特征。

图S8. 图像显示与PC1和和PC2相关的白质和灰质效应。
为了检验PC(主成分)与不同认知领域的行为症状之间的对应关系,作者计算PC变化与ADOS沟通、ADOS社交和ADOS刻板行为评分之间的相关性。第一个PC与ADOS沟通(τ342=0.09, p=0.017)和ADOS刻板行为评分(τ342=0.10,p=0.023)之间呈正相关,但与ADOS社交(τ342=0.06,p=0.136)不呈正相关。第二个PC与ADOS沟通(τ342=0.08,p=0.039)呈正相关,但与ADOS刻板行为(τ283=−0.06,p=0.155)或ADOS社交(τ343=−0.04,p=0.259)不呈正相关。这个结果暴露出的一个局限性是它依赖于相对粗糙的行为度量,需要对涵盖广泛认知能力的更细的行为进行测量,以识别解剖维度和更具体的症状之间的关系。这可能有助于澄清,例如,在第二个PC中,与社会认知相关的区域的体积变化的重要性(见图S9,第一个PC中Broca区(左额下回)的体积变化)。
先前的研究发现,ASD被试和TC被试之间的神经解剖学差异随年龄的变化而变化(18-20岁),在之前内容中作者也报道了ASD特异性特征确实与年龄相关(图1)。然而这并不是ASD特异性个体差异的最大来源:前两个神经解剖学PC与年龄无关(PC1:τ468=0.06,p=0.064;PC2:τ468=0.04,p=0.159)。要想解释清楚ASD中与年龄相关的差异需要更敏感的分析,可能涉及到纵向数据,这在检测年龄相关的差异方面更精确。
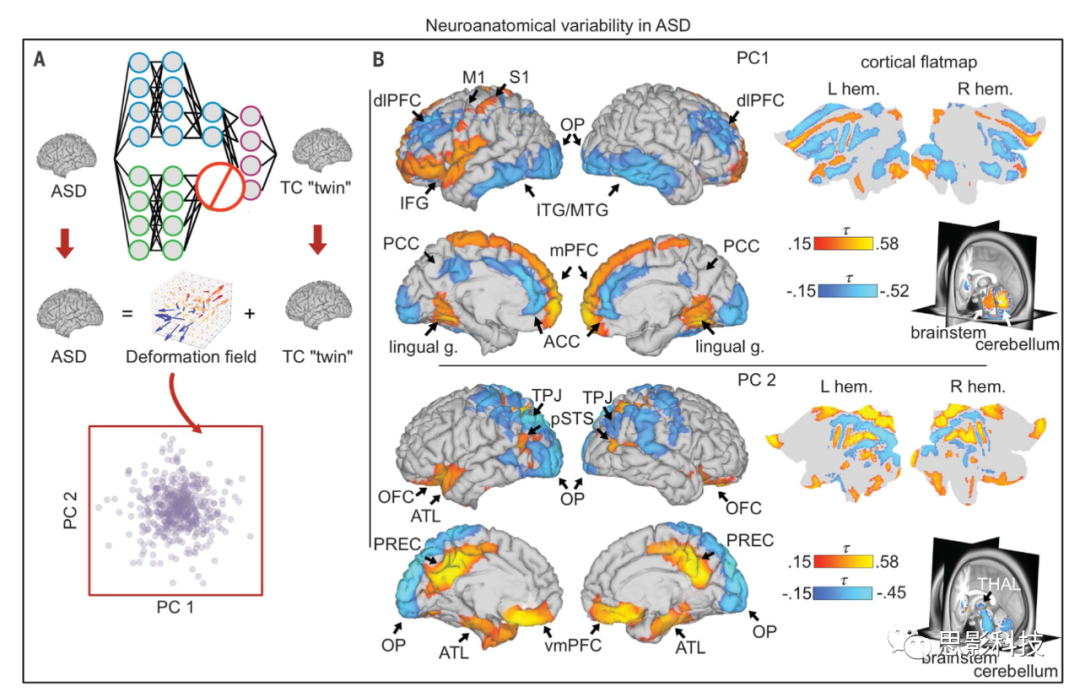
图2. ASD组内个体变异的解剖位点
(A)对于每个ASD被试,作者计算了一个匹配ASD共享特征的合成TC双胞胎大脑,并将其改变为相应的ASD大脑,获得一个变形场。然后,作者将PCA(主成分)应用于被试之间变形场的雅可比矩阵行列式。
(B)区域显示体积增加(红色)和减少(蓝色)与两个PC相关,白质效应报见图S8。
讨论
本文结果表明,使用CVAE方法可以将神经解剖学中ASD特异性变异从共享变异中分离出来,揭示了大脑结构水平上的个体差异与症状和遗传差异之间的相关性。作者可以将该方法推广到新的数据集,并且不需要额外的训练,该特点可以推进此方法在ASD诊断中的应用,在诊断过程中,可以使用训练好的模型分析来自新被试的数据。在本研究中,作者使用CVAE来分析ASD被试的神经解剖学数据,但是该方法也可广泛适用于其他精神疾病其他类型的数据(如行为数据、功能成像等)。
ASD内的个体变异比连续维度更好地捕捉到多个不同的簇,这表明至少在神经解剖学水平上,维度方法可以比离散诊断方法更好地解释个体变异性。然而,功能成像或遗传数据仍有可能揭示神经解剖学数据中不明显的簇。
之前研究表明,与ASD相关的神经解剖学变化在不同的年龄段是有所不同的(18-20岁)。在本文中作者发现年龄不仅与典型对照组共有的解剖特征相关,而且在一定程度上与ASD特异性特征相关,这与ASD特异性的年龄依赖性解剖变化模式相一致。在之前的研究中已经假设了体积变化的多种可能的原因,包括细胞增殖或体细胞大小和树突长度的差异。解释体积变化的结构原因和功能重要性仍然是人类神经科学中一个关键的问题。
神经科学中CVAE的研究前景
研究精神疾病个体差异的细胞基础可能需要新的数据集来验证,包括通过高分辨率成像获得的数据集。CVAE是一种通用的方法,但是高分辨率的数据可能会引起由自编码器处理的数据集的规模方面的挑战。然而,对GPU的改进大大增加了可用内存,最近引入了新技术进行多个GPU的并行计算,使得将CVAEs等深度学习方法应用于规模越来越大的数据集成为可能。
如需原文及补充材料请添加思影科技微信:siyingyxf或18983979082获取,如对思影课程及服务感兴趣也可加此微信号咨询。另思影提供免费文献下载服务,如需要也可添加此微信号入群,原文也会在群里发布,如果我们的解读对您的研究有帮助,请给个转发支持以及右下角点击一下在看,是对思影科技的支持,感谢!

微信扫码或者长按选择识别关注思影
非常感谢转发支持与推荐
欢迎浏览思影的数据处理业务及课程介绍。(请直接点击下文文字即可浏览思影科技所有的课程,欢迎添加微信号siyingyxf或18983979082进行咨询,所有课程均开放报名,报名后我们会第一时间联系,并保留已报名学员名额):
核磁:
上海:
第三十一届磁共振脑网络数据处理班(上海,10.28-11.2)
第六十九届磁共振脑影像基础班(上海,11.4-9)
南京:
第六十七届磁共振脑影像基础班(南京,9.15-20)
第五届弥散磁共振成像提高班(南京,9.22-27)
第三十三届磁共振脑网络数据处理班(南京,10.16-21)
第二十二届磁共振脑影像结构班(南京,10.24-29)
重庆:
北京:
第六十八届磁共振脑影像基础班(北京,9.21-26)
第十届脑网络数据处理提高班(北京,10.20-25)
第十一届磁共振ASL(动脉自旋标记)数据处理班(北京,11.3-6)
脑电及红外、眼动:
重庆:
第四届脑电机器学习数据处理班(Matlab版本,重庆,9.24-29)
上海:
第二十五届近红外脑功能数据处理班(上海,10.17-22)
北京:
数据处理业务介绍:
思影科技弥散加权成像(DWI/dMRI)数据处理
思影科技脑结构磁共振成像数据处理业务(T1)
思影科技定量磁敏感(QSM)数据处理业务
思影科技啮齿类动物(大小鼠)神经影像数据处理业务
思影科技灵长类动物fMRI分析业务
思影数据处理业务三:ASL数据处理
思影科技脑影像机器学习数据处理业务介绍
思影科技微生物菌群分析业务
思影科技EEG/ERP数据处理业务
思影科技近红外脑功能数据处理服务
思影科技脑电机器学习数据处理业务
思影数据处理服务六:脑磁图(MEG)数据处理
思影科技眼动数据处理服务
招聘及产品:
思影科技招聘数据处理工程师 (上海,北京,南京,重庆)