帕金森患者在手臂伸展时可能会出现不同程度的复发性震颤。来自罗马大学的Alfredo Berardelli等人在Movement Disorders发文,旨在探讨初级运动皮质在复发性震颤中的作用,并与静止性震颤进行比较,研究复发性震颤的病理生理学。
招募复发性震颤和静止性震颤两类帕金森患者,分析两类震颤的皮质神经相干性和格兰杰因果关系、在M1区域TMS产生的震颤复位以及刺激运动皮质产生的TMS诱发电位。
本文所用缩略语较多,为方便读者查询,在这里集中列出,其中re-emergent tremor和corticomuscular coherence为核心,给出解释:
RET:re-emergent tremor, 复发性震颤,RET定义为保持手臂伸展时至少3秒后出现的体位性震颤。
CMC:corticomuscular coherence,皮质神经相干性,CMC 指的是大脑皮层区域和肌肉神经活动的同步性。
CSD:电流源密度。
TMS:经颅磁刺激。
EEG:脑电。
EMG:肌电。
TEP:TMS诱发电位。
MEP:运动诱发电位。
M1:初级运动皮质。
ECR:桡侧腕伸肌。
RI:震颤复位指数。
结果:RET表现出明显的皮质神经相干性,以及运动皮质活动与震颤肌肉和震颤复位的因果关系。经颅磁刺激诱发电位的P60成分在震颤抑制时振幅降低,在RET前恢复,在RET(复发性震颤)发作时增强,在RET过程中恢复到与静止性震颤相似的值。与静止性震颤相比,RET表现出与静止性震颤相似的皮质神经相干性和震颤复位性,但频率略高于静止性震颤。
结论:RET与M1的活动有因果关系,M1可能是网络中产生RET的汇聚节点。复发性震颤和静止性震颤具有共同的病理生理机制,运动皮质在其中起着至关重要的作用。
关键词:临床神经生理学、运动皮层、帕金森、TMS-EEG、震颤
1前言:
伴有静止性震颤的帕金森患者可能在手臂保持在伸展位置时出现一种震颤,即所谓的复发性震颤(re-emergent tremor,RET)。临床观察提示,RET可能具有与静止性震颤相似的机制。
只有一项研究调查了RET病理生理特性,发现汇聚在感觉运动皮质上的网络可能参与RET。更好的理解RET病理生理特性可能会开辟一种治疗策略。
在本文中,研究者利用神经生理学技术研究了M1在RET中的病理生理作用,分析流程如下:
1. 利用皮质神经相干(corticomuscular coherence,CMC)研究M1与RET过程中肌肉活动的可能相关性,并试图通过电流源密度(Current source Density,CSD)分析确定其皮层发生源。
2. 计算信号之间的格兰杰因果关系(Granger causality),研究M1和肌肉活动之间任何显著相关性的方向性。
3. 为了进一步探讨M1活动和RET之间可能的因果关系,测量TMS对RET复位的能力。
4. 为了研究M1兴奋性和RET之间的联系,还结合TMS和EEG来研究不同震颤条件下M1刺激产生的TMS诱发电位可能变化。
5. 最后,为了测试M1是否同样参与产生RET和静止性震颤,研究者在同一患者中比较了两种震颤的CMC、格兰杰因果关系和震颤复位。
2方法
被试
帕金森患者(6男,67 ±11岁)(表1),由运动障碍专家、神经科医生根据国际标准确认为帕金森病,振幅分数为≥2的为复发性震颤 (UPDRS 3.15),振幅和稳定性总分≥4的静止性震颤(UPDRS3.17和3.18),且震颤仅限于一侧。RET定义为保持手臂伸展时至少3秒后出现的体位性震颤。排除标准是:有其他神经或精神疾病病史;晚期帕金森病。帕金森病的治疗在至少实验前12小时停止。
表1 患者的人口学特征和临床特征

实验设置
患者坐在专为TMS(EMS,意大利)设计的椅子上,前臂靠在扶手上。在所有的实验中,评估静止性震颤:要求患者将他们受影响的手悬挂在扶手的边缘,并仅在震颤出现至少10秒时进行记录。评估RET:要求患者伸展手腕,同时将前臂保持在扶手上以避免疲劳。
实验:CMC(皮质神经相干性)和格兰杰因果
32导兼容TMS电极帽记录EEG:Fp1-Fp2-AFz-F7-F3-Fz-F4-F8-FC5-FC1-FCz-FC2-FC6-T7-C3-Cz-C4-T8-TP9-CP5-CP1-CP2-CP6-TP10-P7-P3-Pz-P4-P8-O1-O2-Iz。POz电极作为参考,FPz电极作为接地。通道阻抗保持在5kΩ以下。用连接到双极通道的一对Ag/AgCl表面电极记录桡侧腕伸肌(ECR)的肌电图(EMG)。EEG和EMG滤波:DC-3.5 kHz,并使用TMS兼容系统(Neurone,Bittium,芬兰)以10 kHz采样。在三个1分钟的RET和静止性震颤期间记录EMG和EEG。
预处理
在FieldTrip中用自定义脚本实现函数。EEG和EMG信号被分割成3.4秒的时间段,采样频率降到1kHz,去噪,陷波滤波(45-55 Hz),带通滤波:EEG数据1-45 Hz,EMG数据20-250 Hz。从分段两侧剔除200毫秒的数据,以获得3秒的时间段。
利用FastICA算法对EEG信号进行独立成分分析,去除了与肌肉、眼动和电极噪声相关的伪迹。然后将脑电信号变换到头皮表面电压分布(电流源密度变换,“CSD变换”),以减小容积传导效应,提高空间分辨率。用“CSD”工具箱计算CSD变换。然后利用预处理后的时间段进行时频变换,计算1~45Hz频段的EMG和EEG功率谱和交叉谱密度。CMC测量了两个信号在频域中的线性相关性,计算方法为两个信号的交叉谱密度除以每个信号的自谱密度(auto-spectral densities)。在所有EMG通道和EEG通道频谱估计的相同频率范围内计算CMC。
统计
当C3(右颤)和C4(左颤)处的CMC值超过95%置信区间的上限时,根据以下公式进行独立假设,认为其具有显著性:
95% CL = [1-0.05^1/(number of epochs-1)]
在Fieldtrip中计算肌电信号的非参数谱密度估计值与C3(右震颤)或C4(左震颤)的脑电信号之间的格兰杰因果关系。显著格兰杰因果关系的阈值是通过创建1000个EMG和EEG数据集的排列来计算的,在这些排列中,试验顺序被随机打乱,从而产生随机的格兰杰因果值。然后将真实的Granger因果值与随机分布数值进行比较,以检验显著性水平为P<0.05的零假设。
对CMC峰值进行2 (震颤:RET vs. 静止性震颤)×2 (频率:震颤频率 vs. 双倍震颤频率)的重复测量方差分析;对格兰杰因果峰值进行2 (震颤:RET vs. 静止性震颤)×2 (频率:震颤频率 vs. 双倍震颤频率)×2(方向:M1-肌肉 vs. 肌肉-M1)的重复测量方差分析。
实验二——Tremor Resetting震颤复位
与实验1相同记录EMG,但使用D360(DigiTimer,英国)并通过CED 1401 A/D接口以5 kHz频率采样。使用Magstim 2002刺激器连接一个8字线圈(Magstim,Whitland,UK),在震颤对侧的M1处发出单相、单脉冲TMS(SpTMS),从而激发ECR中最大的运动诱发电位(MEP)。将线圈与头皮相切,以诱导垂直于中央沟的前后方向电流。神经导航(Softaxic,EMS,意大利)用于监测线圈位置。刺激强度设置为使用在静息状态下诱发1 mV振幅的MEP的强度。通过5组spTMS分别评估RET和静止性震颤的复位情况,每组包括8个试次,试次间隔在7.5秒到12.5秒之间随机变化。每组之间有30秒的休息时间。
预处理
使用SIGNAL(版本5,CED,UK)分析震颤复位的EMG数据。测量TMS之前5次震颤爆发的峰值时间,得出相应的4个周期长度(CL1-4),并计算平均震颤周期长度(A)。测量从第5次震颤爆发到TMS的时间,并以平均震颤周期长度的百分比(A%)表示。计算TMS之后5次震颤爆发的预测峰值时间,和TMS之后5次震颤爆发的预测峰值时间与实际峰值时间之差(D1-D5);在计算震颤复位指数(RI)时,在5个不同的图上分别绘制了D1-D5与同一试次A%的关系图。TMS之后5次爆发的RI(RI1-RI5)作为RET和静态震颤的5个D1-D5曲线图的回归线的斜率。每个参与者的最终震颤复位指数计算为RI1到RI5的平均值。震颤复位稳定性按RI1/RI5比值计算。
统计
通过计算TMS后5次震颤爆发的平均复位指数(RI)来评估震颤复位(图1)。通过单样本t检验,当RI值与假设平均值零有统计学差异时,震颤复位被认为是显著的。通过测量TMS后第一次和第五次震颤发作之间的RI比值来衡量震颤复位的稳定性。当RI1/RI5比值与假设均值1无统计学差异时,震颤复位被认为是稳定的。使用配对t检验比较RET和静止性震颤之间的RI和RI1/RI5比值。

图1 震颤复位分析。
(A)同一患者的RET(上)和静止性震颤(下)的单一EMG试验中的震颤复位测量示例。CL1-CL4,周期长度;A,平均震颤周期长度;A%,从第五次震颤爆发到TMS的时间(占A的百分比);D1-D5,TMS之后预测的峰值时间与实际峰值时间之间的差异。
(B)一个患者的震颤复位指数(RI)。数据点代表RET(黑色圆圈)和静止性震颤(灰色方块) 的一个试次。根据RET(黑线)和静止性震颤(灰线)回归直线的斜率计算TMS后5次震颤的RI。
实验三—TMS-Evoked Potentials
脑电记录与实验1相同,在线滤波(DC-3.5 kHz),右震颤时采集FC5-FC1-C3-Cz-CP5和CP1,左震颤时采集FC2-FC6-C4-Cz-CP2和CP6,采样频率为80kHz。POz为参考电极,FPz为接地电极。研究者将TEP记录限制在感觉运动皮质的6个通道上。使用双相刺激器(Magstim SuperRapid2)来产生具有短刺激间间隔的TMS脉冲(见下文)。刺激器被连接到一个8字线圈上,以在M1热点上传输双相spTMS,其强度等于活动运动阈值的80%,定义为在持续自愿伸腕(手和前臂之间的0°)期间,在10次试验中有5次产生MEP≥200μV的最低刺激强度。TMS每500毫秒±15%一次,持续60个blocks,包括静止性震颤、腕关节伸展和RET。使用这个短的刺激间间隔来获得高时间分辨率来探测与不可预测的潜伏期现象(RET发作)相关的皮层动力学。使用噪声掩蔽,并在线圈和头皮之间放置了一层薄薄的泡沫,以避免TMS诱发的听觉和假设性体感反应对TEP的污染。
预处理
在Matlab(R2017b)上使用带有Fieldtrip、EEGLAB和TESA函数的自定义脚本进行TEP分析。根据前面描述的方法对EEG进行预处理。10个EMG和EEG数据围绕TMS脉冲(-500到500ms)分段。脑电基线校正(-100至-5ms),并去掉-5 ms-15 ms数据以去除伪迹。信号采样频率1000 Hz。然后,使用FastICA算法对EEG伪迹进行了两轮独立分量分析。在第一轮ICA中,只删除了代表TMS诱发肌肉的大伪迹和衰减伪迹。信号被认为是伪迹的情况:
1)如果它们的振幅明显大于神经信号(>20 uV),2)如果它们具有可能需要>50ms才能恢复的指数衰减型信号,因此抵消了潜在的神经信号。在大约25%的参与者中,肌肉和衰减伪迹作为一个单一成分被消除。在第二轮ICA中,只删除由于电极移动和噪声带来的成分。在不到15%的受试者中,电极移动和噪声伪迹被分离为一个ICA成分。对数据进行凹陷滤波(45~55 Hz)和带通滤波(脑电数据为1~100 Hz,肌电数据为20~250 Hz)。将C3/C4作为局部周围电极的重参考。[C3重参考=(C3-FC1)+(C3-FC5)+(C3-CP1)+(C3-CP5)][C4重参考=(C4-FC2)+(C4-FC6)+(C4-CP2)+(C3-CP6)]。运算符产生在C3/C4水平上记录的TEP的正交源导数,从而减少相邻区域中的源的贡献。
TEPs 条件:基于对EMG的视觉观察,EEG数据根据以下条件被分类:
1) ‘rest tremor’:静止性震颤期间的TMS,
2) ‘posture–onset’:紧跟在手腕伸展之后的第一个TMS脉冲,
3) 'posture–holding’:在完全抑制静止性震颤的同时保持手腕伸展,直到RET发作前1秒的所有TMS脉冲,
4) 'RET onset minus 2',
以及5) 'RET onset minus 1':手腕伸展期间RET开始前的最后两个TMS脉冲,分别为RET开始前1秒至500ms(minus 2)和500ms至50ms(minus 1),
6) 'RET–onset’:紧跟在RET开始之后的第一个TMS脉冲,以及7)‘RET’:RET期间的TMS脉冲(不包括'RET–onset’脉冲)。对每种情况下的EEG信号进行平均和校正,以获得最终的TEP。对于每个受试者,我们计算了所有条件下的总平均TEP,并对其进行了肉眼检查,以确定TMS后前三个峰值的潜伏期。峰值幅度为对应于峰值潜伏期±3ms的恒定时间间隔内的最大值。
TEP trials:为了匹配不同条件之间的试次数量,使用了60个随机选择的无伪迹试次来计算C3通道上“静止性震颤”和“RET”条件下的平均TEP,而所有的无伪迹试次都用于其他条件。用于计算TEP的平均试验次数为57.9±1.8。在每种情况下用于计算TEP的平均试验次数为:‘rest tremor’ 60 ± 0;‘posture–onset’ 57±0.5;'posture–holding’ 55± 0.7;'RET onset minus 2' 57± 0.3;'RET onset minus 1' 58± 0.2;'RET–onset’ 58± 0.2;‘RET’ 60 ± 0。

图2 TEPs方法。
(A)TMS EEG设置。右主震颤(左图)和左主震颤(右图)患者在绕圈通道的TMS过程中分别记录脑电数据。
(B)每组模块包括:(1)静止性震颤10s,然后(2)自愿伸腕(可变持续时间),最后(3)复发性震颤(RET),10s。(C)TEPs条件。竖条表示在1个示例期间传递TMS的时间范围;标签显示TEP条件是如何基于ECR肌肉的EMG定义的。
统计
根据对肌电图的目测,EEG试验可分为下列情况:(1) rest tremor, (2) posture onset, (3) posture holding, (4) RET-onset minus 2, (5) RET-onset minus 1, (6) RET onset, and (7) RET (图2). TEP是通过对每种情况下的脑电数据进行平均得到的。然后根据Hjorth参考技术将C3/C4通道上的TEP转换为正交源导数,以减少来自M1以外的源的污染并进行校正。分析仅限于C3/C4通道和早期TEP,因为最近的TMS-EEG研究表明它们分别在感兴趣的区域和时间内,这最能反映M1局部兴奋性的变化。从posture onset至RET onset的RET平均潜伏期为5.44±0.76秒(3.2~9.4秒)。
数据正态性采用Shapiro-Wilk检验。以震颤条件(7类,见上)和TEPs成分(P30,N45,P60)为主要因素,对TEPs波幅进行双因素方差分析。进行多次配对t检验作为post hoc分析,错误发现率校正阈值为0.1。采用Spearman‘s等级评定震颤抑制期间TEP变化: 1-[姿势保持/静止性震颤])与RET潜伏期之间的相关性。
3结果
皮质神经相干性及格兰杰因果
RET肌电主峰位于4.74±0.13 Hz(震颤频率),次峰位于9.40±0.22 Hz(双倍震颤频率)。RET对侧C3/C4上的EEG在RET频率(4.60±0.12 Hz)处出现一个峰值,在双倍震颤频率(9.40±0.22 Hz)附近出现第二个峰值。所有患者在RET期间均在震颤频率和双倍震颤频率出现明显的CMC。
静止性震颤肌电在4.27±0.14 Hz出现主峰,8.73±0.27 Hz出现次峰。静止性震颤对侧C3/C4的脑电在静止性震颤频率(4.30±0.15 Hz)处出现一个峰值,在双倍震颤频率(8.50±0.31 Hz)附近出现第二个峰值。在静止性震颤时,所有患者在震颤频率和双倍震颤频率下均表现出明显的CMC。在震颤频率和双倍震颤频率下,RET的肌电频率均明显高于静止性震颤(见图3A)。在双倍震颤频率下,RET的脑电频率峰值明显高于静止性震颤,但在震颤频率下仅有向更高频率移动的趋势,见图3B。方差分析显示震颤×频率交互作用不显著。双倍震颤频率下的CMC显著高于震颤频率(0.146±0.02 vs 0.106±0.01),具有显著的频数主效应(P=0.024)。RET时CMC值在震颤频率(0.09±0.01 vs 0.12±0.12)和双倍震颤频率(0.12±0.02 vs 017±0.02)均低于静止性震颤,但无显著性差异。RET和静止性震颤的地形图均显示最大CMC值在震颤对侧的中央外侧皮质之上。与静止性震颤相比,RET显示CMC值分布稍宽,向顶叶皮质后方延伸更多(图3C)。6例RET期间和4例静止性震颤时M1-EMG方向的G-因果关系在震颤频率下显著,而在双倍震颤频率下,除1例患者外,其余患者均在两类震颤中均显著。在震颤频率下,8例患者RET与10例静止性震颤在EMG-M1方向上存在显著的G因果关系,而在双倍震颤频率下,仅有1例患者在两次震颤中均有明显的G-因果关系。G因果关系方差分析显示方向×频率交互作用显著,单独的震颤、频率、方向主效应均不显著,方向×震颤、频率×震颤、方向×震颤×频率交互作用均不显著。Post hoc分析显示,在震颤频率下,M1(初级运动皮质)-to-ECR(桡侧腕伸肌)方向的G-因果关系显著低于ECR-to-M1方向,而在双倍震颤频率下,G-因果关系在M1-EMG方向上更高,图3D。

图3 CMC和格兰杰因果关系。阴影区域,标准误差;虚线水平线,统计显著的阈值。
(A)ECR肌肉的肌电功率谱。
(B)左侧震颤患者在震颤频率RET(I)、震颤频率静止性震颤(II)、双倍震颤频率RET(III)和双倍震颤频率静止性震颤(IV)的CMC谱和地形图。
(C)C3/C4通道的脑电功率谱。
(D)格兰杰因果谱。
Tremor Resetting
平均1 mV MEP强度为最大刺激器输出的68%±8%。图1显示了1例有代表性的受试者的数据。RET的平均RI与0相比有显著性差异(2.07±0.10,P<0.001),而RI1/RI5比值与1相比差异无统计学意义。静止性震颤的RI也有显著性差异(2.16±0.17,P<0.001),RI1/RI5比值与1相比差异无统计学意义。配对t检验显示RET与静止性震颤的RI和RI1/RI5比值均无统计学差异。
TMS-Evoked Potentials
C3处的TEP在不同条件下的平均峰值时间分别为28.1±0.2、45.5±0.4和63.0±0.6毫秒,分别与前面描述的分量P30、N45和P60一致(图S2)。经Shapiro-Wilk检验,各状态下峰值波幅均呈正态分布(P>0.05)。方差分析显示条件(7类)、成分(P30,N45,P60)和条件×成分交互作用的主效应显著。随访单因素方差分析显示P60成分存在简单的条件主效应,其原因是静止性震颤时P60波幅(2.43±0.04)显著高于posture holding (0.71±0.15)和RET-onset minus 2 (1.05±0.29),RET onset的P60幅度(4.69± 0.76)显著高于rest tremor (P = 0.003), posture onset (2.01±0.4), posture holding (P < 0.001), RET-onset minus 2 (P < 0.001), RET-onset minus 1 (2.61 ±0.49), 和RET (2.42±0.52)。不同条件对P30和N45波幅无显著影响,见图4和图s3-s4。posture holding时P60抑制与潜伏期呈显著正相关(P < 0.001; Fig. S5)。

图4.TMS-诱发电位(TEP)结果-Hjorth参考。
(A)TMS后,在4种典型条件下,电极C3/C4处的总平均整流TEP。垂直线表示rest tremor (红色)和RET onset(蓝色)的P60波幅。阴影区域,标准误差。
(B)不同条件下的P60平均振幅。*Post hoc significant versus rest tremor; §post hoc significant versus RET onset。有关POz参考的结果,请参见图S3。用POz和Hjorth参考分析TEP结果相似。
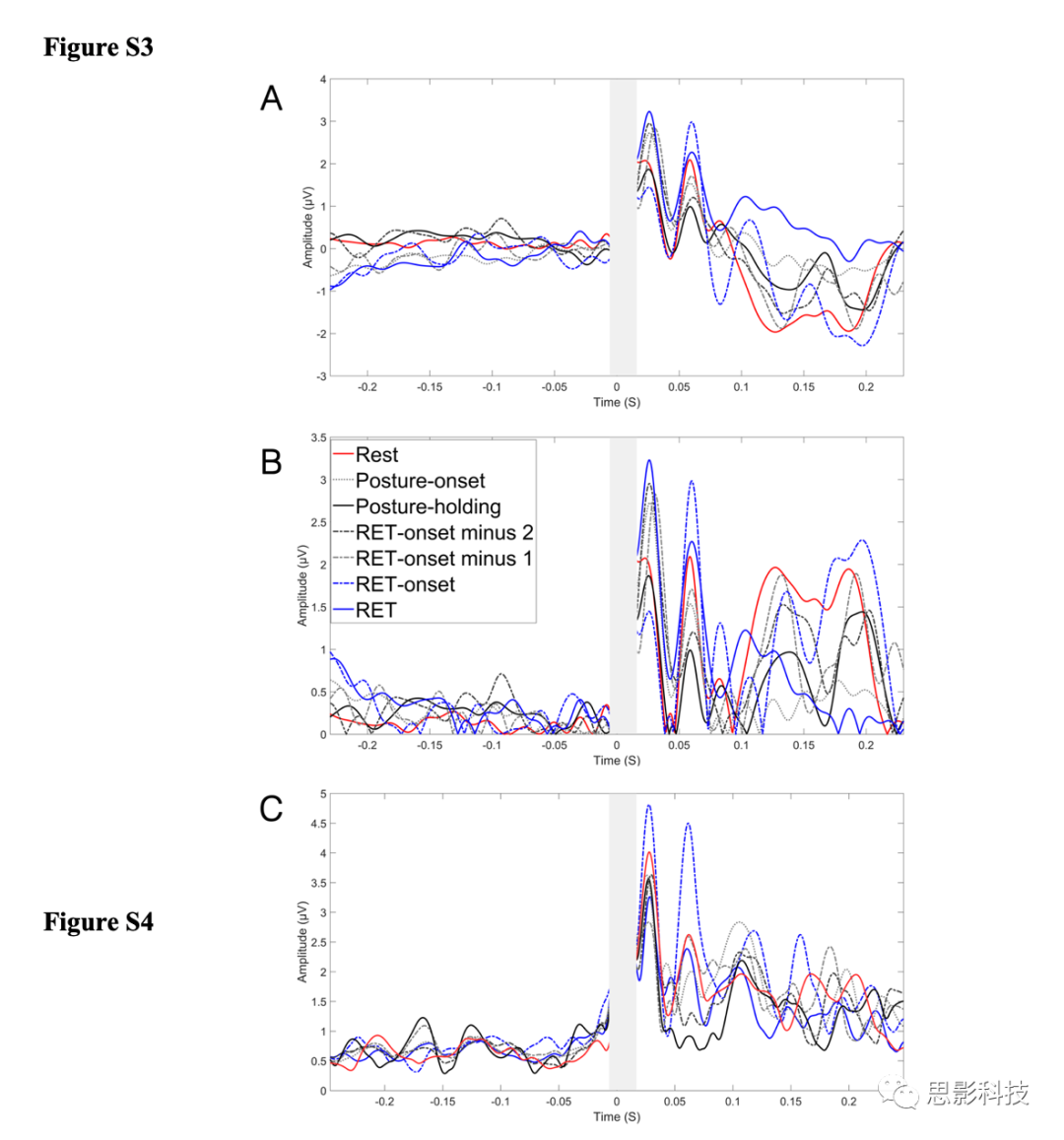
图S4 TMS-诱发电位(TEP)结果-补充。
A)原始TEP;
B)在C3通道水平上不同实验条件校正后的TEP;
C)电极C3/C4通道上的校正TEP,平均所有受试者(n=10)。灰长条:内插信号。45 Hz低通滤波器用于平滑TEP以用于绘图。

图S5 P60抑制与RET潜伏期的相关性。P60抑制表示为(1-(‘posture–holding’/‘rest tremor’)),RET潜伏期从‘posture–onset’到 ‘RET–onset’。
4讨论
本研究的第一个结果是,在RET过程中,EMG和EEG的活动在震颤频率上是一致的。研究者在对侧感觉运动皮层对应的脑电图电极上定位了与RET一致的振荡活动来源。震颤分析还显示,在RET和静息状态下,第二个CMC峰值在大约两倍的震颤频率处。以前的研究曾将这第二个峰值解释为技术伪迹或生理现象。G因果关系表明,在震颤频率下,信息传输是从肌肉到M1的方向上,而在大约两倍的震颤频率下,主要是在M1到肌肉的方向上。这些结果表明,震颤频率的皮质-肌肉神经耦合主要反映肢体运动产生的本体感觉输入;而双倍震颤频率的耦合反映的是参与驱动震颤的M1输出。
在M1之上的TMS产生震颤复位,这不能完全用与MEP诱发相关的感觉反馈来解释,而是通过皮质-皮质下连接(如超直接通路)干扰M1皮层内或基底神经节的活动解释。然而,以前的证据已经将震颤复位与M1皮层内机制直接联系起来,从而限制了震颤复位通过激活M1到基底神经节连接获得的可能性。研究者发现TMS后第一次震颤爆发的复位与TMS后第五次震颤爆发的复位相似,表明复位是稳定的,而不是暂时性的。发现的稳定复位表明,对M1进行的TMS通过将RET产生网络的振荡活动设置到其周期中的一个新的固定点来直接影响RET产生网络,而瞬时复位则表明振荡器本身没有受到影响。因此,稳定的复位表明M1是皮质-皮质下网络中产生RET的非常关键的节点,而不仅仅是输出。最后,复位的结果表明,RET起源于涉及M1的网络活动的不稳定性,并且不是来自一个独立的振荡器。
在伸展手腕抑制震颤的过程中,TEP P60的波幅降低。P60在震颤再次出现前完全恢复,并在RET开始时被增强。然而,在震颤过程中,RET发作时观察到的P60增强作用消失,P60波幅恢复到与静止性震颤相似的值。一些证据表明,由M1 TMS产生的TEP是皮层兴奋性和连接性的一个可重复性的指标。在正常人中,P60主要分布在中央前回,后部向躯体感觉皮质扩散,其幅度受TMS刺激设置的影响,TMS刺激设置能反映M1的兴奋性和感觉输入。
本研究提供的TMS低于诱发MEP的阈值,由于肌肉抽搐,P60调制不能用感觉反馈来解释。作者发现RET潜伏期和姿势保持期间P60抑制之间的直接相关性可能表明P60调制反映了与震颤相关的M1兴奋性的变化。因此,P60波幅变化在不同实验条件下反映不同神经生理特性的可能性不大。尽管最近有证据表明RET潜伏期与RET波幅呈负相关,而本研究发现P60在RET开始时波幅最大,此时震颤波幅最小。因此,作者认为P60调制反映了与震颤直接相关的M1兴奋性的变化,与其幅度无关。在这种情况下,P60的减少表明在震颤抑制过程中M1的抑制;当P60恢复时,震颤以RET的形式返回,这表明M1的兴奋性在震颤产生网络中起着非常关键的作用。RET潜伏期的M1抑制可能是由于皮层内抑制增加或姿势改变通过脊髓小脑通路影响小脑-丘脑-皮质网络而引起的本体感觉输入。类似地,RET开始时M1的促进可能表明皮层内促进作用增强,或者它可能首先出现在GPi,该核被认为通过M1激活小脑-丘脑-皮质回路来“开启”震颤。
最后,通过对同一患者的RET和静止性震颤的比较,提供了新的发现。研究结果发现RET和静止性震颤有相似的EMG峰、EEG峰、CMC和G因果关系。然而,与静止性震颤相比,RET显示震颤峰的EMG频率稍高,且稍宽的CMC分布向顶叶皮质延展。可能是由于与静息状态相比,肢体机械共振不同的中枢振荡器相互作用所致。事实上,RET和静止性震颤频率之间的微小差异可能来自不同的本体感觉输入,这些输入与肢体在姿势保持和休息期间的不同机械条件有关。相应地,在RET中,CMC向顶叶皮质延伸的不同分布表明,躯体感觉输入的贡献更大。因为RET和REST震颤的复位数量和稳定性相似,结果表明M1在RET和REST震颤中起着相似的作用,复位很可能是通过一个共同的中心振荡器的扰动实现的。
减少实验偏差的几项预防措施:排除有头部震颤的患者(机械运动会影响EEG)以避免CMC(皮质神经相干性)分析中的偏差。根据最新的标准进行TMS脑电检查,以最大限度地减少非经颅TMS相关诱发电位对TEP的污染。此外,在实验期间保持TMS参数的一致性,任何可能受到感官电位的污染在震颤条件下都是稳定的,不能解释观察到的TEP的调制。由于皮质脊髓的激活,如震颤复位,因此TMS刺激幅度在运动阈值以下诱发TEP以限制偏差。
5、结论
(1)在RET过程中,EMG和EEG的活动在震颤频率上是一致的。在EEG和EMG峰值之间存在显著的皮质神经相干。
(2)震颤频率下的格兰杰因果在肌肉到M1方向上占主导地位,而在双倍震颤频率下,它在M1到肌肉方向上占主导地位。
(3)在M1位置上进行TMS引起RET的显著复位。
(4)M1处的TEP记录显示,posture holding和RET出现期间的静止性震颤抑制与TEP P60的显著调制有关。
(5)与静止性震颤相比,RET的肌电频率略高,但两种震颤的皮质神经相干和格兰杰因果值相似,TMS后的复位也相似。
请微信搜索“思影科技”关注我们,关注我们的公众号,获得更多精彩脑科学内容,如需原文或对思影科技课程感兴趣请添加微信号siyingyxf或19962074063
微信扫码或者长按选择识别关注思影
非常感谢转发支持与推荐
欢迎浏览思影的数据处理课程以及数据处理业务介绍。(请直接点击下文文字即可浏览思影科技所有的课程,欢迎添加微信号siyingyxf或19962074063进行咨询,目前思影采取预报名制度,以下所有课程均可报名,受疫情影响部分课程时间或有调整,报名后我们会第一时间联系,会为您保留名额):

第二十八届磁共振脑影像基础班(重庆2.24-29)
第十四届磁共振脑网络数据处理班(重庆3.18-23)