大约20%的创伤性颈髓损伤会导致四肢瘫痪。目前很多研究正在开发针对性的神经修复方法,以应对这种情况,从而改善患者的生活。但是在目前的很多研究中,要么使用穿透性的方法来对皮层放电信息进行解码,带来很多颅内感染风险以及多次更新编码问题,要么使用非侵入性的头皮外采集方法(类似于脑电采集),这种方法带来的缺陷是能够对外骨骼或者帮助设备支配的自由度低。因此,为了对上述问题的解决进行更好的探索,来自法国格勒诺布尔大学的研究者测试了一种新的脑机结构的概念模型。
本文中,作者的目的旨在测试通过大脑信号驱动外骨骼(外骨骼是一种由钢铁的框架构成并且可让人穿上的机器装置,这个装备可以提供额外能量来供四肢运动,使用大脑信号驱动可以大大提高这种技术的应用能力的半侵入性技术的可行性)(颅脑由外到内,分别是头皮,颅骨,硬(脑)膜,蛛网膜,软膜,大脑。硬膜外是介于颅骨和硬膜之间的空隙)。
方法:
作者招募了法国格勒诺布尔大学医院的两名研究中心的参与者参加他们正在进行的临床试验。纳入标准是年龄在18-45岁之间,其神经功能缺陷稳定、患者表示出额外的活动能力、是否流动或住院监测、并且在法国社会保障系统进行登记并签署了知情同意书。排除标准包括既往脑外科、神经心理后遗症、抑郁、物质依赖或误用,以及脑磁图(MEG)、EEG或MRI的禁忌症。由于植入物的技术问题,一名参与者被排除在外。剩下的参与者是一位28岁的男子,他在c4-c5脊髓损伤后出现了四肢瘫痪。两个双侧无线硬膜外记录器,每个都有64个电极,植入到大脑的上肢感觉运动区域。采用自适应解码算法在线处理硬膜外皮质电(ECOG)信号,向外骨骼发送指令。在整个24个月的研究中,病人做了各种任务,以逐步增加动作的自由度(degrees of freedom,即评价外骨骼进行活动自由的标度)。
发现:
在2017年6月12日至2019年7月21日期间,病人用虚拟化(64.0%[SD5.1]成功)或实验室外骨骼(70.9%[11.6]成功)进行运动,对模拟步行的项目进行了严格控制,并在不同的触控任务和手腕旋转中进行了八个自由度的双侧、多关节、上肢运动。与微电极相比,硬膜外ECOG具有半侵入性,且有相似的效果。解码模型可重复使用大约7周,无需重新校准。
解释:
这些结果显示,使用连续的在线硬膜外ECoG来解码大脑活动的完整的脑机接口可以系统的长期(24个月)的激活四肢神经假肢外骨骼。在使用中,使用者的活动最多可以达到8个自由度,并且可以连续使用长达七周。
引言
颈脊髓损伤后,大约20%的人患有四肢瘫痪。感觉运动障碍的程度取决于脊髓病变的类型。治疗方法旨在恢复活动和改善生活质量。已经有研究成功地使用了神经修复术和脑-计算机接口来绕过脊髓病变,使用功能性电刺激,对动物或人的肌肉,或脊髓,或使用机动神经假肢和其他人体效应物进行重新控制。外骨骼(手矫形器,臂,和下肢外骨骼)已与基于脑电图的脑-计算机接口用于康复,可以用在因中风或脊髓损伤(四肢或截瘫)引起的严重运动障碍患者的神经功能恢复中。感应器可以通过穿透微电极或脑外网格采集来自残余意志功能或脑电活动的触发信号来对其进行控制。自1998年以来,皮层活动一直被用于控制效应物。然而,尽管使用电线微电极记录可以来控制许多动作,例如基于中等控制维度的有线皮质脑电图(Ecog)的短期、半侵入性脑-计算机接口,但临床上仍没有一种可以弥补运动缺陷的解决方案。
本文作者设计了一个方案,为四肢瘫痪患者提供原始的神经假体,由患者的大脑控制,以无监督的方式进行,并满足长期植入装置(无线、完全植入和长期生物兼容)的要求。脑-计算机接口系统包括一个完全植入的硬膜外记录器,64个电极,一个带有四肢的电动外骨骼,嵌入式解码算法和软件。本文介绍了该系统的首次临床应用,并报告了一项临床试验的初步结果,该试验旨在评估设计的系统对四肢瘫患者的安全性、长期耐受性和潜在益处。该报告来自五名计划患者之一的概念验证结果。
被试
作者研究了2名患者。在第一个患者中,在皮肤闭合时,对植入物进行探查、发现短暂激活和停止通信。该病人被排除在研究之外。技术问题在第二位患者植入前就被发现并纠正了。第二位病人是一位28岁的男子,他在c4-c5脊髓损伤后出现了四肢瘫痪(图1a)。患者申请参加作者的试验。在满足标准并提供书面知情同意(通过代理)后,他被纳入方案。病人对上肢几乎没有运动控制。仅通过肱二头肌收缩(美国脊髓损伤协会损伤ASIA评分:4个右侧,5个左侧)、肘部和腕部伸展(0右侧,3个左侧),才可能移动。以下所有其他肌肉在ASIA量表上评分为0,不能执行任何任务。除了这些肌肉,感觉运动障碍是完全的。他用左臂扶手操纵杆控制的轮椅,没有其他辅助技术。另外三名病人也是按照同样的协议招募的。
材料
作者的团队设计了一个植入式记录系统,WIME,用于在感觉运动皮质上双侧硬膜外永久性植入。电子元件放置在一个钛盒(直径50毫米,厚7-12毫米,外凸面)。一组64阵列(90:10)记录电极放置在装置的平面内表面,用来记录硬膜外ECoG(直径2毫米,4-4.5mm螺距,和5个参考电极) (图1B)。一项对绵羊的研究表明,硬膜外的ECOG记录在8个月以上是稳定的。数据是通过超高频天线(402-405 MHz)发射的。电源通过13.56 MHz感应高频天线远程供电.,两个天线都被嵌入在肌肉下面的硅酮折板中。由于受限无线电链路(≤250 kb/s)造成的数据速率有限,每个植入体在586 Hz采样时仅使用32个触点。无线连接使用由定制设计的头盔在记录器前面的两个外部天线。
增强移动性外骨骼(图1c)是一种机器人神经假体,具有可穿戴和完全机动的四肢。该装置重65公斤,设计为由病人解码的硬膜外ECOG脑信号控制。背包计算机接收到硬膜外ECoG信号。这些信号被实时解码。然后每100ms将这些增量发送到外骨骼控制器,并将其转化为产生上肢拟人化运动的运动指令。下肢的激活是通过一个开关来实现的,它控制一个模拟行走的程序。
开发了实验协议、软件和解码算法,并将其集成到自适应脑信号解码器框架软件中,以提供350ms以内的硬膜外ECOG活动的自适应高分辨率解码,类似于健康参与者的反应时间。最初,译码器是一种递归的、指数加权的、n维的偏最小二乘回归算法。为了提高译码稳定性和静止状态支持,后来又增加了马尔可夫切换线性模型。
在既往临床前研究期间开发了自适应解码算法和软件(图2,3),并在使用MEG的术前临床研究(NCT02790411和NCT02790424)中进行了测试。自适应解码器允许快速校准和高速在线解码信息。

图1:临床数据、记录仪和外骨骼。
(A)患者的运动控制和灵敏度均低于红色的曲线水平。脊髓损伤稍微不对称,右侧(c4:仅c5以上的二头肌和肌肉受自愿控制)较左侧(c5:患者可收缩二头肌和腕屈肌)更为严重。两侧感觉图相似(C4)。MRI表现为脊髓广泛的严重病变(脊髓总萎缩伴脊髓空洞症)。颈椎进行仪器固定。
(B)生物兼容无线WIME记录仪是为慢性植入而设计的。
(C)外骨骼被设计为模仿人体形状及其移动性的可穿戴的人形通用神经假体。外骨骼是自我支持的,无线的,自主的2·5小时。平衡行走不可用也不可实现,但可通过软件(VectorEliteModel[Bioness,Valencia,CA,USA])实现。密勒密=增强迁移率。
程序
在MEG和fMRI下,患者上肢和下肢进行了真实或虚拟的运动。每次运动重复100次(随机4-6s间隔),用于MEG和fMRI扫描为80次(随机10-20s持续时间)。
使用1.5T的MRI(西门子;图4A,附录P2),检测到感觉-运动皮层神经元在任务期间的活动;图4A,附录P2),生成fMRI图像(使用SPM的3D图)以确定目标的空间坐标。使用306通道ElektaNeuromag MEG(ElektaOy,赫尔辛基,芬兰)获得MEG图像(图4B,附录p2)。(思影科技将开展脑磁图数据处理相关课程,如感兴趣,请联系微信号:SIYINGYXF进行咨询)
使用融合的fMRI-MEG图像,使用了图像引导下的外科手术镜(图4)来定位被认为是感觉运动皮质的中心作为颅骨切除的目标中心。
使用CT(Symbia[西门子医疗系统)在术后观察电极网格和颅骨,提供解剖学和功能的(MRI-CT)配准(图4C,4D,附录P2)。WiMagine记录器不是MEG或MRI兼容的,因此,使用CT进行了该项操作。
手术及术后方法
手术在全身麻醉下完成。作者使用图像引导SURGISCOPE软件进行神经导航(图4D),以双向植入感觉运动皮层上方的记录器(图4C,D)。半侵入性的(与穿透记录方法相比)使用(5cm直径颅骨切开术)和硬膜外放置可以预防颅内感染,因为没有电极穿透大脑,整个过程没有完全嵌入的设备和无线连接(包括在任务期间)。在最终皮肤缝合之前和之后,使用无菌袋中的天线,术中记录硬膜外麻醉信号,评估植入物的手术损伤程度。手术后不打算取出记录器,但必要时除外。
开始2分钟内进行硬膜外麻醉记录,以监测体力变化信号质量(幅度、信噪比、伪影的存在)。大脑-计算机接口任务用于校准、训练和评估性能和进度。要求患者在心理上触发ON-OFF开关或进行连续任务。
通常,实验包括两个阶段:第一是校准以创建或更新解码器,而第二阶段是解码器用于估计其性能的使用。当模型的性能被声明为满意时,可以重新使用模型而不需要更新新的session。作者评估了三种不同类型的任务的性能;一个为期4周,2个为期7周。(图5)。

图2:实时数据处理
(A)在脑-计算机接口和任务执行(例如,单肢目标到达)期间,同时记录硬膜外ECOG(每个WIME植入记录器32个通道),手的位置和腕关节旋转的坐标,以及行走的大脑开关的状态。在586Hz采集硬膜外ECOG数据。
(B)在标定和训练阶段,提取时间(T)的手运动特征:矢量距离(从y1、y2和y3坐标到目标到达任务的坐标)、角度(腕部任务前角位置与旋后任务时目标角位置之间的夹角)和行走的二元变量。
(C)应用ccwt(Morlet)提取硬膜外ECOG特征。
(D)将提取的特征的10-15s长数据存储在具有用于移动的数据的临时缓冲器中。该信息用于创建每10-15s更新的模型。该模型更新所需的中间数据累积所需的信息仅存储在运行存储器中,在实验期间具有10-15s长数据的特征提取。每0.1秒,利用前1个记录中提取的特征,由模型和相应的控制命令进行在线预测,并将相应的控制命令发送到效应器。CCWT=复连续小波变换。
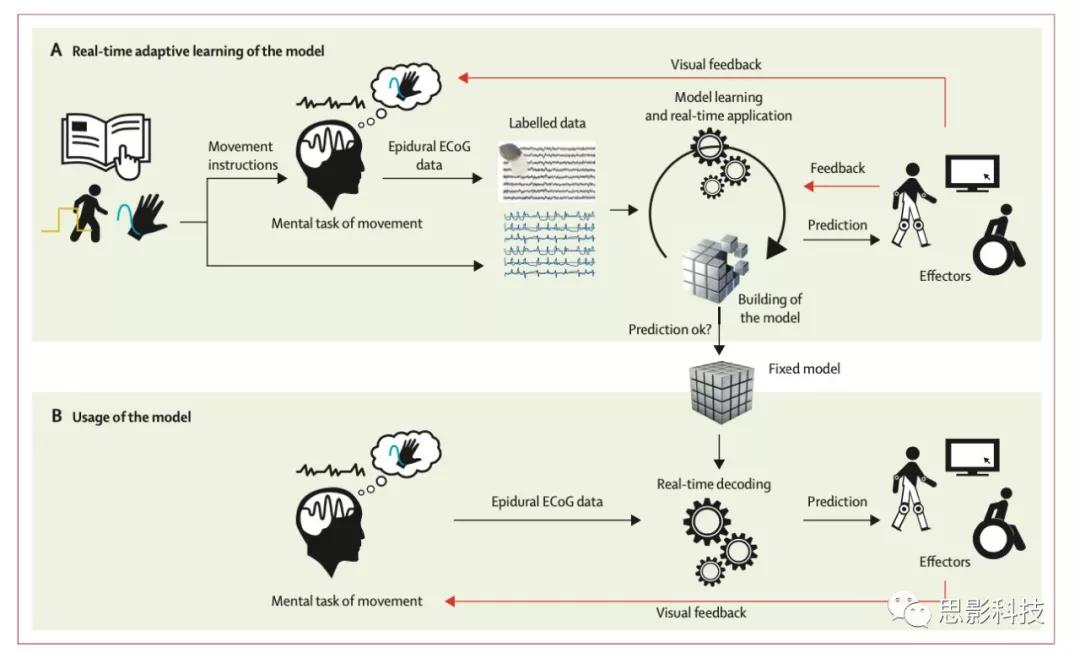
图3:实时自适应学习策略
(A)指令被传达给病人,病人创造了一个运动的心理任务,在他的感觉运动皮层产生神经活动。该活动由Wimagine记录为硬膜外麻醉数据,该数据被发送到解码器。ABSD软件分析了这些数据和生成的命令以驱动马达并移动患者或化身的肢体。在整个过程中使用了自适应模型学习和实时应用。该过程为患者提供了视觉反馈(红色箭头),并且在校准阶段仅向解码器提供运动反馈(红色箭头)。对初始记录周期的分析产生第一解码模型。当病人完成训练任务时,这个模型被迭代更新(每10-15秒)。最后一个模型预测了在线和实时(350 ms以内)特定任务的特性。当预测被认为是足够的时候,实验者终止了模型的建立,并认为它已经准备好使用了。
(B)当病人创造一项新的心理任务来诱发运动时,由他的感觉运动皮层产生并由WIMIME记录的硬膜外ECOG数据由最终模型实时在线解码。所需的运动被解释,命令被产生并传达给执行者(例如,外骨骼的马达),因此它们可以开始相应地移动四肢。由此产生的动作为病人提供了视觉反馈,使他能够在执行下一个动作时调整自己的心理任务。ABSD=自适应脑信号解码器。
患者在诸如视频游戏之类的各种效应器上心理上触发开关事件,以启动人体模型行走。
患者对上肢进行连续的空间运动,结合三维转换和手臂旋转,包括一维单向运动(游戏涉及脑力控制桨以拦截掉下的球,类似乒乓)、2d运动(视频游戏涉及在虚拟的黑色面板上到达和触摸目标),或佩戴外骨骼,并使用指尖与两侧的8个发光二极管(LED)进行交互,用于双臂、3D和多肢体运动(使用化身或外骨骼,以与两侧16 LED的面板互动),被试还进行了第4d(自由度)和多肢运动(三维位移加腕关节旋转[60°绕臂轴向任意方向旋转])。
完成该组任务后,要求患者增加两个上肢(每个4个自由度)和下肢(开关)的自由度。该控制允许参与者自由地移动每个臂。
对于心理开关任务,病人的成功率为一个真阳性率(即正确动作在尝试次数中所占的百分比)、每分钟的假阳性(即每分钟不想要的动作数)或假阳性率(不想要的动作或休息期间的动作百分比)。作者还计算了曲线下的接收操作特性曲线(ROC)和面积(AUC;附录P5)。对于所有接触和触摸会话,作者计算了REACH的成功率和R比率(计算为指尖与目标之间的距离与实际距离),以及它们随时间的变化(图5)。每一项任务的难度在整个研究过程中都保持不变。在适当的情况下进行简单的统计分析(平均[SD])。根据一段时间内达到的自由度,对患者的进展情况进行了调查(图5)。同时,患者在家中与一名研究人员进行的培训(TC;95天)加强了在实验室使用外骨骼所获得的任务和技能(45天)。

图4:感觉运动皮质的皮层定位和手术
基于(a)fMRI和(b)Meg的手术前策略被设计为识别精确的手术目标。
(C)将fMRI和MEG数据结合起来,确定最活跃的感觉运动皮层目标(白色圆圈)的坐标,中心集中在Rolandic沟附近(红色)。
(D)这些坐标被转移到图像引导手术镜。手术过程中拍摄的照片显示在闭合头皮之前植入植入物;手术后的X线片显示其最终位置(远离中线上的上纵向凹陷)。M1=初级电动皮层。S1=主要感觉皮质。Bold=血氧水平相关。MEG=脑磁图。
结果
2017年6月12日患者被招募,2017年6月21日接受手术,随访于2019年7月21日(正在进行)。在本研究开始之前,参与者使用了轮椅,并具有非常小的电机控制。然而,他的fMRI和MEG记录显示,当想象自己移动他所有的四肢时,产生皮层信号的能力很强。作者的结果表明,随着时间的推移或重复,病人对每项任务的内在表现都有了明显的改善。从这个临床试验中,作者既没有观察到也没有预料到病人的缺陷的临床改善。随访时未见不良反应。
研究期间未发生术中或术后并发症。在操作完成整个系统功能后1天进行硬膜外麻醉记录。第15天观察到的高信号幅度(13.7/Vrms[SD4·47])在第30天至第379天的手术后(18.7/Vrms[6.54])再吸收后增加。第15天之前由带宽(从34.9dB到4.6dB(100:200Hz)归一化)归一化的信噪比(dB)也从第30天至第379天增加(从0:10Hz到5.0dB(100:200Hz))。感觉运动皮层的长期、高质量的硬膜外麻醉记录允许患者通过各种学习步骤进行进一步控制。
为了实现外骨骼的高维控制,自由度从大脑的转换逐渐增加到8自由度。对解码器进行定期校准和更新。对模型的可用性进行了三次测试,在长时间内不进行校准或更新,在项目早期使用化身在4周内行走,在最近的任务中,被试控制化身在7周内完成了8自由度的测试。最初的解码器在手术后的第10个月和第16个月进行了两次更新(图5)。
在行走任务中,患者达到了真正的阳性有效率82.5%(SD8·6),假阳性率12.5%(5.9),18项实验中的AUC0.78(0.14);视频游戏:真实阳性率92.1%(4.3),假阳性4.9(1.9)/min,AUC0.84(0.05),1个月没有重新校准,15个任务中的AUC为0.84(0.05)(图5、6a)。
术后2个月6个实验中,佩戴悬吊外骨骼时真阳性率为72.6%(15.3%),假阳性率为7.1(5.6)/min,AUC为0.84(0.06)。总距离为145米(39个阶段的480步行走)[图5,6a;视频4]。化身下肢的开关控制也被成功地用于触发每条腿的独立运动以及交替的双足活动。Roc曲线见附录(P5)。
对于涉及上肢控制的乒乓球游戏任务,患者在使用左手进行的19个实验中达到54%(SD 12.7)(图6b,视频1)。在目标任务中,病人用左手完成2d任务成功率为:17次实验,80%(15.5)成功,比率2.8[1.4]),用右手完成的成功率为:19次试验,82.2%[12.0]),成功率3.3[1.5];图5,6c;附录p4)。在目标任务中,病人用左手(7次实验,56.9%[15.3]成功,6.8[4.1])和右手(11次实验,52.5%[11%]成功,6.6[3.6];图5,6d;附录4)都能基本完成3D任务。
该训练计划的最后一部分是化身的多肢体激活,以生成同时控制多个自由度的组合任务的模型。患者进行二维、双手(7次试验,69.6%[SD 6.1]成功,3.8[1.5];图5,6e;附录p4)和三维双手任务(6次实验,57.2%[9.5]成功,6.3[3.2]次);图5,6F;附录p4,视频2)。最后,患者使用相同的模型完成5个8D的任务,在7周内没有重新校准。
在外骨骼触觉操作中,患者用左手(两次实验,68.9%[SD 1.1]成功,5.7[2.4])或右手(1次实验,61.5%成功,6.1[2.5]次;图5,6d;附录4)完成了三维任务。
外骨骼训练方案的最后一部分是外骨骼的多肢激活,以生成同时控制多个自由度的组合任务的模型。患者完成2d双手任务(成功率83.8%,比8.4[4.7];图5,6e;附录p4)和三维双手任务(成功率71.4%,比5.3[1.4];图5,6f;附录p4)。最后,患者用同一模型完成5个8D任务,7周以上(70.9%[11.6]成功,比率9.8[3.5]。在5次三维任务中完的完成率达到99.2%[1.8]成功率,比率4.0[1.0];图6g,附录p4,视频3)。
在手术后立即完成了CT扫描。使用Tap finger Psychomotor Target (NCT02790411,NCT02790424)范式。病人运用单个关节的运动意图来显示手-腕-指表象与虚拟动作之间的对应关系。下肢活动与与上肢活动相关但仍远离半球间裂缝的下肢活动相关(图1B、4)。运动意图与由fMRI检测的硬膜外麻醉和氧消耗所检测到的神经元活动有关。与脑-计算机接口解码相关的一组触点,与硬膜外麻醉和fMRI信号定位一致(附录P3)。

图5:递增维数的累积性能
时间线显示超过20个月的DoF数量的发展(实心黑线),虚线黑线表示未包括在本文中的任务(20-24个月)。显示ABSD更新的标签(红色方格)。在第10个月中,初始算法rew-npls与mslm相结合。16月龄时,对高维控制参数进行修改。没有重新校准的周期被描绘出来。比率列表示从原点出发到达目标的距离(DT)在实际原点与目标距离(dOT)上的比值。
DoF=degreesof freedom. FP=false positive.
FPR=falsepositive rate. MSLM=Markov switching linear
model.REW-NPLS=recursive,exponentially weighted, n-way, partial least squares.
SVG=serious video game. TPR=truepositive rate
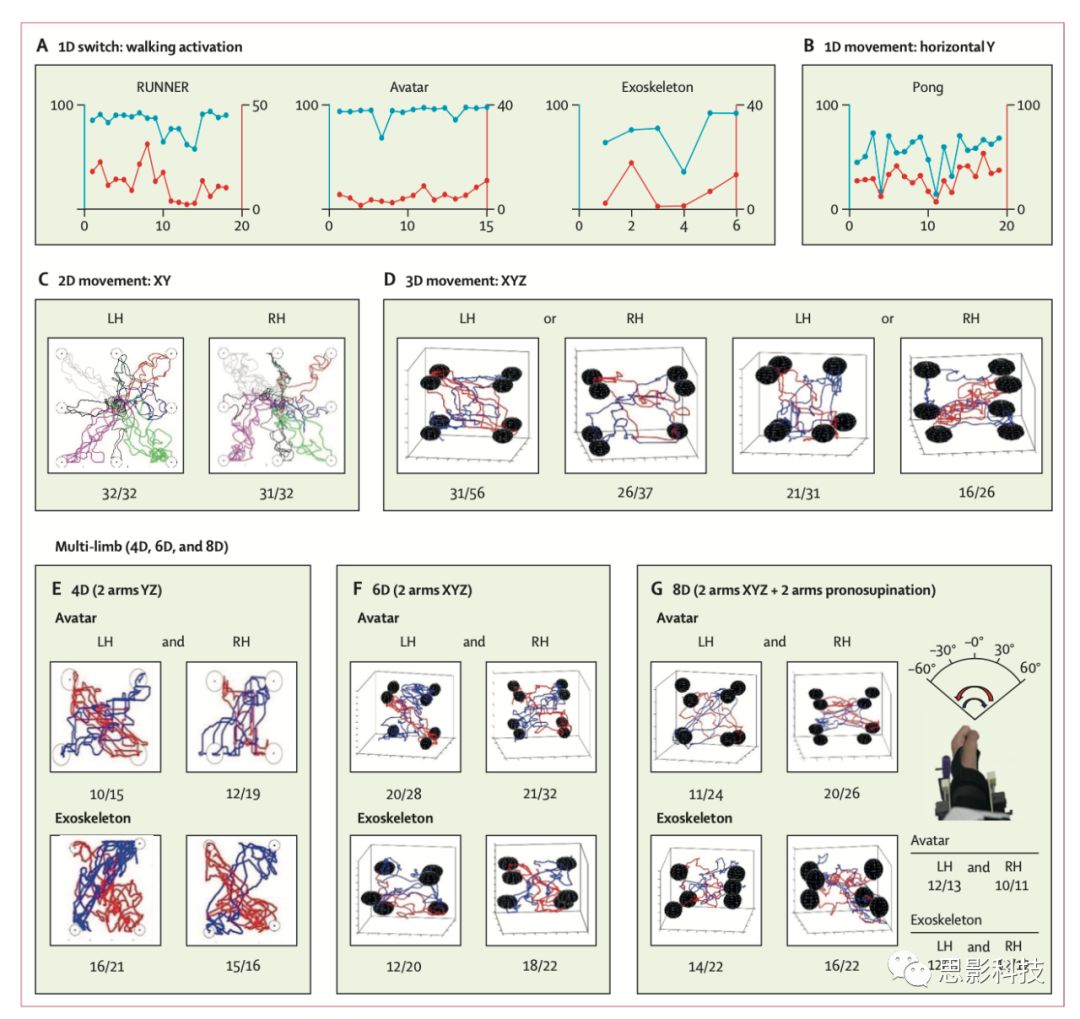
图6:运动任务的累积结果
1D任务通过
(A)激活开关(运行电子游戏、控制化身或外骨骼)或作为
(B)一维位移(乒乓游戏水平轴)来完成。对于触发步行启动的开关,结果可分为真阳性激活(真阳性率占预期激活次数的百分比[蓝线])和随机假阳性激活(运行视频游戏的假阳性率或阿凡达和外骨骼的每分钟假阳性率[红色曲线])。在乒乓球游戏中,根据落地球被划桨拦截时的命中率(蓝色曲线,y轴)和落球数(红色曲线,y轴)来判断成功与否。
(C)2d任务涉及到在一个虚拟的家庭表示法中,用手在一个正方形上触及8个目标。
(D)使用手在立方体上触及16个目标所涉及的3D任务。
(E)多肢4d工作,包括用双手在两个平板上触及8个目标。
(F)多肢6d任务涉及使用双手在两个立方体上触及16个目标。
(G)使用双手在两个立方体上达到16个目标所涉及的多肢8D任务。该任务是用与6D任务相同的设置完成的,其中增加了手腕的旋后(在任一方向上60°),这增加了每只手的一个自由度。
(c-g)中的图表显示了在一个任务期间累积的实际轨迹,使用左手和右手,以及在所呈现的数字上达到的目标数。使用家中的化身和实验室的外骨骼执行(d-g)中的所有任务。
讨论
这项研究描述了第一次成功的长期使用无线硬膜外多通道记录器对四肢瘫痪患者进行肢体康复的治疗过程。在本研究中,所有长期人类临床应用所需的技术要素(硬膜外记录、无线功率和发射、多个ECOG通道的在线解码以及完全嵌入)被首次结合起来。许多双侧电极的长期组合使作者有可能探索多肢的高维控制。作者的干预措施没有显示信号退化,没有副作用,也没有持久的耐受性。这项研究显示了作者所使用的系统,其容量大,使用的硬膜外的ECOG记录的数据能够实现在线和实时地解码,同时,在不需要几个星期的重新校准情况下,其性能的降低也很小。
控制维度从步行任务逐步增加到8d(自由度)双任务。从自适应实时线性解码器到自适应实时非线性动态译码器,采用后续算法实现了对多肢的异步控制。这个概念的第一个临床证明,证明作者的系统可以从实验室扩展到家庭环境和其他应用。
8自由度的成功控制(病人可以永久进入所有维度)、手术植入后24个月的步行能力以及在没有重新校准的情况下几个星期后的继续控制是迄今为止所报道的最高成绩。
使用侵入性微电极记录的病人报告了最佳的高维控制(机器人手臂的10d控制)。然而,由于生物相容性问题和安全问题,这种系统的长期应用受到限制,并且需要进一步的技术发展以使它们与人类的长期使用相容。此外,还有研究报道了用微电极记录的局部场电位的长时间(2~5个月)稳定开关解码在四肢瘫痪患者中的应用。其他解码器也能够在无需再训练几天的情况下进行高维控制,且只有20-50%的性能下降。尽管进展良好,但不稳定的校准仍然限制了基于微电极记录的脑-计算机接口的临床应用。
硬膜外ECOG记录器覆盖比微电极记录装置覆盖更大的皮质表面。种植体的不变空间定位防止了重新校准的需要。作者研究的最初目标得以实现,证明大脑-计算机接口技术可能涉及到高水平的复杂性,例如控制全身外骨骼。外骨骼是一种仿生拟人化神经假体,可能是完全补偿四肢瘫痪患者损伤的最佳方法。本研究中使用的外骨骼不允许平衡地自主行走。下一个目标是解决病人自我调节行走的问题。同时,证明四肢瘫患者可以用大脑来控制神经假体效应,同时结合多个自由度,可能会将这一概念扩展到更高水平的控制。这一延伸将允许患者仅使用大脑活动(视频5)驾驶轮椅,最终导致四肢瘫痪患者逐步融入家庭、城市和职业环境。作者的病人已经认为他快速增加的假肢移动性是值得的。然而,这一进展并没有改变他的临床地位。本报告的主要目标是表明,控制四肢骨骼外骨骼的双侧、半侵入性、硬膜外慢性植入物可以是患者更接近于在弥补缺陷方面取得预期的进展。
这些系统的进一步研究还将有助于我们更好地理解大脑功能,因为该研究分析了在任务期间触发的皮层事件。未来的研究将提供关于感觉运动皮层持续能力作用的信息,这实际上是产生实现真正运动所需要的信号。在一些情况下,使用外骨骼比使用替身的性能要好,平均高10%-20%。这一发现可能是由于反馈和病人感知的差异所致。在带有化身的2d屏幕投影中,直接(且仅)反馈是视觉的,因此需要额外的认知努力来概念化第三维度。在外骨骼的真实环境中,病人在现实世界中得到了更丰富的反馈。
病人在训练过程中的改善是由于他对人工神经的控制能力的改善,还是由于他的大脑或智力的提高,目前尚不清楚。尽管任务成功率有增加的趋势,触控任务的比率也有下降的趋势,但作者无法确定是否发生了神经改变,因为模型是定期重新创建的,算法也得到了改进。由于达到了8自由度的控制,模型7周没有改变。下一阶段的试验旨在记录脑-计算机界面培训期间的学习过程。
作者的结果提示,该系统能够准确地利用几个皮质区域的信息,以在残疾人中重建某种程度的辅助移动性。与运动意图有关的硬膜外ECOG活动的热点与通常在感觉运动皮层上的表现相对应。有趣的是,这项研究可能支持训练诱导的神经可塑性假说,在未使用的皮质区域开发新的功能。虽然下肢表现隐藏在半球间,但最强烈的下缘相关硬膜外ECOG活动通常记录在初级感觉皮层的最内侧接触处。这种活动可能通过横切的内质纤维从初级运动皮层传播,或通过长距离检测与下肢活动有关的硬膜外ECOG活动进行传播。或者,皮质区可以由邻近的运动神经皮层响应于来自前额叶皮层的功能压力而被激活。在初级感觉皮质上的电极表现的这种明显扩展还可以支持运动皮层表现出多种模态的感觉响应,包括视觉和躯体感觉。因此,这些研究将提供有关感觉运动皮层从皮层持续能力产生作用的信息,以产生实现真实或虚拟运动所需的信号。

微信扫码或者长按选择识别关注思影
第十四届磁共振脑网络数据处理班(重庆,7.26-31)
第三十届磁共振脑影像基础班(南京,7.31-8.5)
第十届脑影像机器学习班(南京,6.30-7.5)
第十二届磁共振弥散张量成像数据处理班(南京,6.18-23)
第二十届脑电数据处理中级班(重庆,8.9-14)
如对思影课程感兴趣也可微信号siyingyxf或18983979082咨询。觉得有帮助,给个转发,或许身边的朋友正需要。请直接点击下文文字即可浏览思影科技其他课程及数据处理服务,欢迎报名与咨询,目前全部课程均开放报名,报名后我们会第一时间联系,并保留名额。
小动物磁共振脑影像数据处理班(预报名,南京)
第二十一届脑电数据处理中级班(南京,9.7-12)
第七届眼动数据处理班(南京,7.26-30)
脑电信号数据处理提高班(预报名)
脑磁图(MEG)数据处理学习班(预报名)
思影科技功能磁共振(fMRI)数据处理业务
思影科技弥散加权成像(DWI/dMRI)数据处理
思影科技脑结构磁共振成像数据处理业务(T1)
思影数据处理业务三:ASL数据处理
思影科技脑电机器学习数据处理业务
思影数据处理服务五:近红外脑功能数据处理
思影数据处理服务六:脑磁图(MEG)数据处理
招聘:脑影像数据处理工程师(重庆&南京)
BIOSEMI脑电系统介绍
目镜式功能磁共振刺激系统介绍