促进脑卒中患者运动功能的恢复,优化康复策略,与个体化预测的挑战密切相关。经颅磁刺激(TMS)和脑电图(EEG)的联合应用已被证明能在个体水平上记录局部和网络反应。为阐明TMS-EEG评估卒中后运动恢复的潜力,作者对28例卒中患者用神经导航的TMS-EEG对患侧初级运动皮质(M1)进行了检测。在卒中后的早期(6.7±2.5天),TMS诱发的EEG反应在患侧M1区域上表现出两种明显不同的反应形态。在损伤较轻的患者中,TMS引起了分化和持续的EEG反应,并在两侧大脑半球均依次出现一系列偏转。这反映了在健康对照组中观察到的双侧激活模式。相比之下,在另一组受严重影响的患者中,TMS引起的局部反应缓慢而简单。在时域和时频域量化TMS-EEG反应显示,与健康对照组相比,卒中患者表现出慢而简单的反应和较高的振幅。重要的是,卒中后的这些活动变化模式不仅与最初的运动障碍有关,而且与卒中3个月后的运动恢复有关。因此,数据显示脑卒中后早期运动网络内的局部效应和因果关系严重受损。此外,对于MEP缺失和临床表型相同的严重受累患者,TMS-EEG提供了不同的反应模式,表明了个体功能恢复的潜力。因此,TMS-EEG支持评估个体反应特征,扩展了脑卒中研究的方法范畴。本文由德国科隆大学学者发表在BRAIN杂志。
小编注:TMS-EEG的实验范式已经成熟,从检测到治疗都有对应的研究,本文作者利用TMS-EEG的一个基本优势“它不依赖于皮质脊髓束或其他传出和传入通路的完整性,而是直接评估皮层的兴奋性和活性”,通过最简单的实验范式,来评估TMS-EEG在卒中后运动功能恢复中的应用价值。虽然实验过程简单,但是作者分析的指标类型丰富,且都有利于得出文章主要想表述的结论,可见作者有深厚而扎实的理论功底。实验中分析的指标和对其的解释值得大家认真揣摩。
重要缩写
ARAT=行动研究手臂测试;
ERSP=事件相关频谱扰动;
LMFP=局部平均场功率;
MEP=运动诱发电位;
M1=初级运动皮质;
MSO=最大刺激器输出;
NIHSS=美国国立卫生研究院卒中量表;
RMT=静息运动阈值;
TEP=TMS诱发的EEG电位
方法
参与者
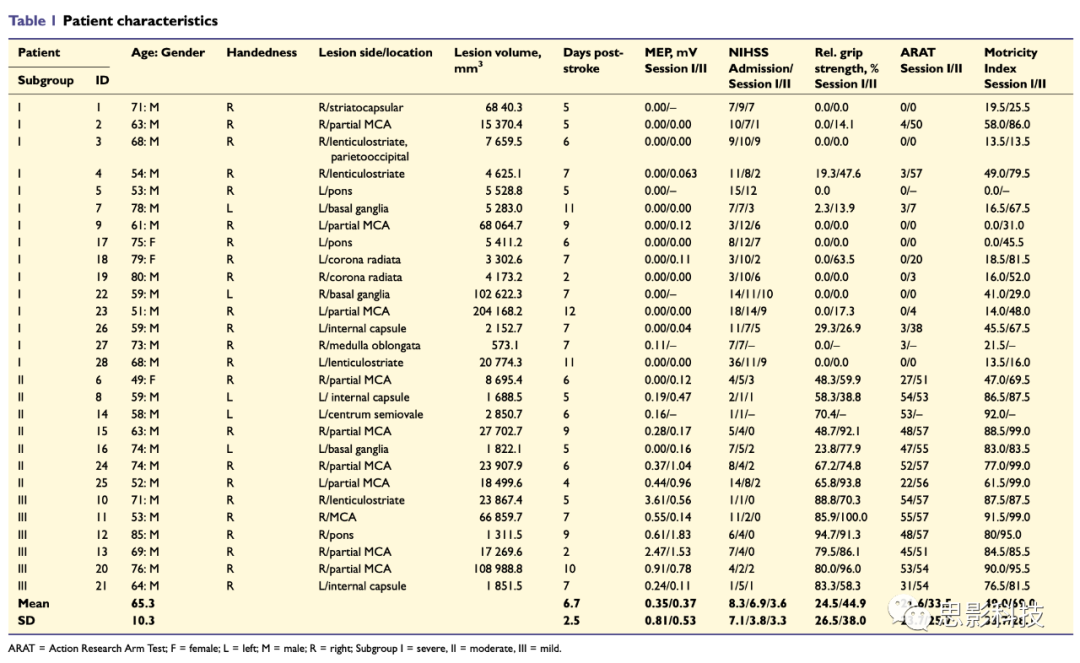
28名住院卒中患者[3名女性,25名右利手,平均年龄65.7±10.1岁范围49-85岁],由于首次缺血性卒中,有轻度到严重的运动障碍[上肢动作研究试验(ARAT):21.6±23.7;0-55;美国国立卫生研究院卒中量表(NIHSS):8.3±7.1;1-36]。
根据以下纳入标准纳入患者:
(i)年龄在40至90岁之间;(ii)经弥散加权磁共振成像(DWI)证实的缺血性卒中;(iii)在亚急性早期阶段,症状出现<14天(卒中后6.7±2.5天;2-12天);(iv)单侧手运动障碍。定义年龄界限是为了招募具有代表性的卒中患者样本。
排除标准是:
(i)TMS的任何禁忌症(如癫痫、心脏起搏器);(ii)双半球梗死;(iii)脑出血;(iv)妨碍签署知情书面同意的认知障碍或失语。参与者的上肢损伤范围广泛,严重或瘫痪的患者比例很高。12例患者上肢无残馀运动功能。16例患者在TMS最大刺激输出(MSO)时未检测到MEP。25名患者在卒中后至少3个月(卒中后132.4±23.5天;99-183天)进行重新评估。
15名年龄匹配的健康参与者,无任何神经或精神疾病史(2名女性,14名右手使用者,平均年龄62.2±13.0岁;51 -76)作为对照组。
表1 参与者信息
运动测试
我们在每个阶段评估四个运动和临床参数:
(i)NIHSS对全局神经损害进行评级;
(ii)运动指数,对手臂和腿部近、中和远端关节的肌肉力量进行分类
(iii)ARAT,评估粗大和精细的上肢功能;
(iv)在连续三个试次中使用握力计分别评估每只手的最大握力。
为了进一步分析,我们计算了一个握力指数,代表卒中患者相对于健手的相对握力:
平均握力(患手)/平均握力(健手) x100
TMS-EEG数据记录
TMS使用Magstim Super Rapid2刺激器。配备Magstim 70毫米8字Alpha胶片线圈。使用无框架计算机化立体定位神经导航系统(BrainSight V.2.0.7)跟踪和记录线圈的位置。(TMS应用于患侧初级运动皮质(M1)。患侧M1的“运动热点(motor hotspot)”被定义为与颅骨呈45°前后方向相切的TMS脉冲的反应,诱发瘫痪手部第一骨间肌肉(FDI)振幅最高的运动诱发电位(MEP)的线圈位置。这种定向在中央沟前壁(相当于中央前回的后壁)的神经元处诱发垂直电流,并优先跨突触激活皮质脊髓系统)
TMS诱发的EEG电位使用TMS兼容64通道EEG系统记录。放大器可防止磁饱和(saturation),并允许在施加TMS脉冲期间连续记录数据。脑电信号采样率为5 kHz,分辨率为0.1 mV/bit,滤波为高通0.1 Hz和低通1kHz。头皮EEG采用62个与TMS兼容的Ag/AgCl电极,安装在弹性电极帽上,按照标准布局和国际10-20系统进行记录。64通道系统中剩余的两个电极被用来记录水平和垂直眼球运动以及眨眼,方法是将一个电极放在左眼外眼角旁边,另一个电极放在右眼下面。
为了优化TMS的兼容性,在整个实验过程中,所有电极的阻抗都保持在5kΩ以下。此外,为了防止EEG听觉诱发电位以及TMS点击引起的眨眼或眼肌反应,参与者佩戴了插入式耳塞。在TMS线圈和脑电极帽之间放置了一层薄薄的塑料膜使TMS产生的骨传导最小化。(小编注:很好的实验指导方案)
实验程序
在每次TMS-EEG之前,评估患侧M1的“运动热点”、MEP状态以及随后的静息运动阈值(RMT)。重要的是,在放置脑电极帽之前确定患者的MEP状态和RMT。然而,由于脑电极帽可能会因为线圈-皮层距离的增加而增加诱发MEP所需的强度,所以在帽后确认或调整RMT。MEP状态通过逐渐增加刺激强度来分类,直到在10个试次中至少有5个试次可以在静止状态下以一致潜伏期诱发任意幅度的MEP。如果没有得到符合这些标准的应答,即使是100%的MSO,患者也被归类为MEP阴性。在可检测到MEP的情况下,用MEP波幅评估患侧M1的皮层兴奋性。为此,在0.2Hz的频率下,用110%的个体RMT诱发10个MEP。如果我们即使在MSO(n=16)的情况下也不能在同侧大脑半球诱发MEPs,则使用对侧RMT作为个体阈值的参考。
这一过程背后的基本原理是为了避免由于损伤诱导的断开效应而导致的虚假的高刺激强度,而不是降低的M1神经元兴奋性。此外,先前的研究表明,尽管患侧大脑半球的皮质运动兴奋性随卒中后的时间和运动损伤的程度而变化,但对侧兴奋性随着时间的推移保持相对稳定,并且与健康参与者没有不同。如果在患侧半球上检测不到MEP,则使用解剖学标志,即hand knob,来定义患侧运动热点。
在EEG记录过程中,将至少100次单TMS脉冲施加于患侧M1的运动热点,随机间隔为6.5-8.0s,强度为RMT的80%,该强度高于EEG反应阈值。此外,阈下刺激强度限制了传入的躯体感觉反馈,这是已知的对EEG反应的影响。在TMS-EEG记录期间,参与者坐在舒适的椅子上,并被要求保持清醒,睁着眼睛。12例因躯干无力而不能坐在椅子上的重伤患者,在床上观察头部倾斜45°,清醒,睁开眼睛。
数据分析
使用MatLab R2017b和EEGLAB进行数据预处理和分析。目测脑电对TMS的反应,以排除单一试次和单一通道的人为干扰。每名参与者至少有90次无伪迹试次用于进一步分析(无伪迹单项试次数:患者:96.8±10.4,健康对照组:97.5±25.0;内插通道数:患者:5.0±1.4,健康对照组:3.9±2.0)。消除相对于TMS脉冲起始的-2ms到10ms之间的TMS伪迹。缺失的数据使用基线替换。随后,对数据进行去线性趋势、带通和带阻滤波(1-60 Hz;49-51 Hz;Butterworth三阶),降采样至625Hz,并在TMS脉冲-1000ms至+1000ms的时间窗口进行分段。对坏通道进行球形插值。采用全脑平均进行重参考并进行基线校正。使用EEGLAB函数runica进行独立成分分析,去除与TMS相关的其他伪迹以及眼动或肌电伪迹。
为了比较患者和对照组患侧M1的局部TMS诱发的脑电活动,我们首先计算了局部平均场功率(LMFP),它将诱发电场量化为时间的函数。基于7例脑卒中患者(图1和图2)的简单双相慢波和持续100ms的大正波的TMS-EEG反应形态,选取两种时间窗内的数据进行后续分析,早期时间窗在+10~+100ms之间,晚期时间窗在+100ms~+200ms之间。
LMFP(局部平均场功率):最接近刺激部位的感兴趣区域(ROI)通道(M1为FC3-FC1-C3-C1-Cz/FC4-FC2-C4-C2-Cz)的TEP平方均值的平方根。然后对LMFP时间序列应用Bootstrap统计(排列数量=1000,α<0.01),以估计与基线(-300ms至-50ms)有显著差异的LMFP值。我们计算了刺激后平均在+10ms到+100ms和+100ms到+200ms之间的显著激活积分。这两个时间段是基于卒中患者的TMS-EEG简单阳性反应(图1和图2)选择的。
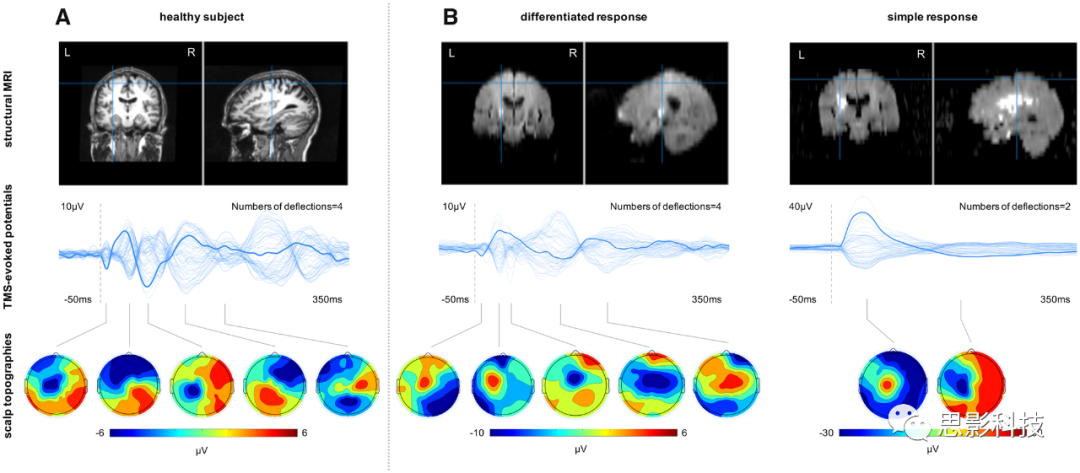
图1 代表性被试对M1刺激的TMS-EEG反应
(A)健康被试。(B)卒中患者。顶行:病变位置。中间行:代表全部62个脑电电极的蝶形图(粗线:刺激电极/C3)。下排:TMS诱发反应的地形图。
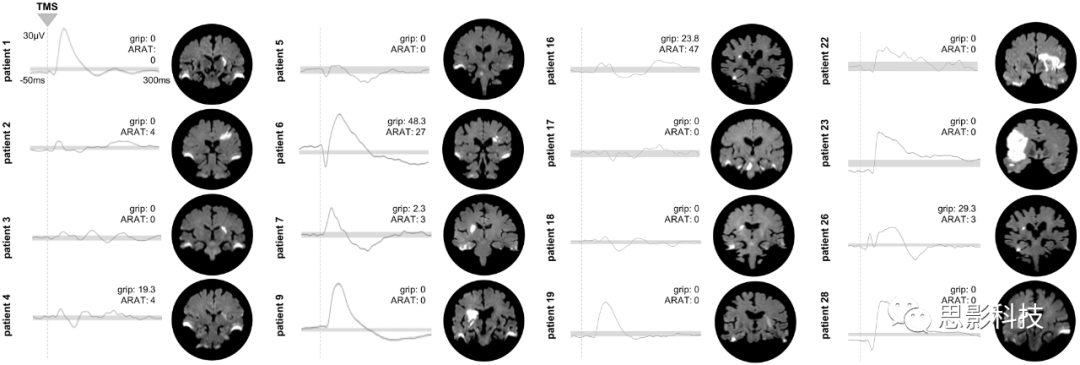
图2 无诱发MEP患者亚组的不同TMS-EEG反应
卒中后早期无MEP的所有患者(n=16)刺激的患侧运动皮质的TMS-EEG反应。灰色条表示99%置信区间。在TEP曲线图旁边,显示了各个患者的相应运动评分。此外,单个弥散加权磁共振成像的冠状位切片显示急性缺血性病变。注意,颞叶的双侧高信号是由易感性伪迹引起的
此外,为了量化健康参与者的高频复现波和患者的低频复现波的不同反应模式,我们考虑了显著偏转的数目作为参考。因此,我们使用bootstrap对刺激前的活动进行了研究,确定了个体被试水平刺激部位下的平均TMS-EEG反应的显著性阈值。
通过基于Morlet小波变换的事件相关频谱扰动(ERSP)计算,得到了时频域的频谱特征。在年轻的健康对照者中,TMS诱发的脑振荡活动的主要频率是特定于刺激部位的。然而,即使不是直接刺激,每个皮层区域也会以从快到慢、从rostral到后脑区的梯度振荡,接近其固有频率。因此,我们从患侧运动皮质、患侧前额叶皮质和患侧顶叶皮质三个不同部位提取了刺激患侧M1时的固有频率,即最大功率频率。
固有频率分析:采用Morlet小波变换(3.5个周期)时频变换后,通过计算事件相关频谱扰动(ERSP)来评价频谱特征。该过程是通过使用EEGLAB函数newtimef实现的。在单试次水平应用绝对频谱标准化,首先执行全长度单试次校正,然后对所有试次的平均ERSP进行刺激前基线校正(-500ms至-100ms)。最后,只有在基于引导的统计数据。排列数量=1000,α水平<0.05)中存留下来的相对于基线的显著ERSP值被考虑用于进一步分析。我们在5-50Hz频率范围和刺激后20ms-200ms之间的时间窗口内对ERSP进行平均,以最大限度地减少刺激时可能出现的伪迹的影响。
统计分析
使用SPSS进行统计分析。使用单样本Kolmogorov-Smirnov检验,首先验证变量是否服从正态分布,以决定参数或非参数统计量。相应地,采用重复测量方差分析和事后t检验或非参数Mann-Whitney U检验进行显著性差异评估(P<0.05)。此外,为了说明非参数统计中的交互效应,我们计算了对齐和秩变换的数据的重复测量ANOVA。
为了阐明组间的显著差异是否依赖于最初的运动症状严重程度,我们使用2Dk-Means聚类,通过早期亚急性阶段的ARAT和相对握力评估,将运动损伤分组,分为轻度损伤(n=6)、中度损伤(n=7)和重度损伤(n=15)三组。
用k-means聚类分析将亚急性期早期的ARAT评分和握力指数分为三类,分别反映轻度(ARAT的聚类中心为45.9,相对握力为79.8%)、中度(ARAT的聚类中心为37.0,相对握力为44.8%)和重度运动损害(ARAT的聚类中心为1.1,相对握力为3.4%)。在这个组分类的基础上,随后使用单变量方差分析和Kruskal-Wallis检验来揭示组间差异。
最后,检验观察TMS-EEG活动变化是否与初始临床损害或卒中3个月后的运动恢复有关。我们使用主成分分析(PCA)计算卒中后第一天的运动综合评分:
(i) 患侧手的ARAT评分;
(ii) 相对握力;
(iii) 患侧手臂的运动指数评分。
NIHSS评分没有包括在内,但用于测试与全局神经损伤的相关性。
为了生成综合恢复分数,我们首先计算每个感兴趣的参数(即ARAT、握力和运动指数)在第一次测试和后续测试之间的相对差值:
d(x,y)=(x-y)/1+y
其中d=差值分数;x=时间点1的分数;y=后续的分数
随后,将z标准化的差值再次输入PCA,其中第一个分量代表上肢的运动恢复。我们还测试了MEP状态与初始损害和恢复之间的关系,以阐明TMS-EEG反应是否增加了MEP的预后价值,特别是对于MEP阴性的患者。以综合康复评分为因变量,初始运动综合评分、MEP波幅或TMS-EEG参数为自变量进行线性回归分析。
由于初始功能损伤会对恢复效果产生影响,因此进行相关分析以说明初始损伤的部分相关。事后检验和相关性才用FDR进行多重比较校正。
基于体素病灶映射(VLSM)
为了评估刺激效应是否与病变部位相关,我们用非参数制图(NPM)软件根据DWI病变范围进行了基于体素病变症状映射(VLSM)。对于所有中风患者,在中风后的前两天内,使用1.5T飞利浦磁共振扫描仪在临床获取磁共振图像标准序列(DWI,T2-加权,T2*加权,FLAIR和血管造影序列)。基于弥散加权成像(DWI)(TR=3900ms,TE=95ms,FOV=230mm,22个轴位,体素大小:1.8x2.99x6 mm3),使用MRIcron软件创建单个病灶图。使用NPM进行了VLSM。只有在至少10%的患者中受损的体素被纳入分析。我们使用推荐用于中等样本量的非参数置换试验(2000置换)进行多重比较矫正。
结果
大脑皮层兴奋性
与健康人(55.0±11.2%MSO)相比,亚急性期和大于3个月的患者患侧大脑半球RMT均明显增高。患者的RMT从卒中后第1周至卒中3个月后显著下降。
然而,在没有MEP的情况下,即使在最大MSO的情况下,对侧M1也可以作为用于TMS-EEG的个体阈值的参考。重要的是,患者和健康对照组之间的实际平均刺激强度没有显著差异。因此,不同群体之间的差异不能用刺激强度的差异来解释。
卒中后TMS诱发皮层活动的特征
评估卒中后2周内卒中患者TMS诱发的脑电,发现TMS触发的反应形态主要有两种截然不同的性质(图1)。在大多数(21名)患者中,TMS在刺激后的300毫秒内,在双侧大脑半球引起一系列正负偏转,并与快速变化的双侧大脑半球激活模式相关,可与健康对照组中观察到的反应相媲美。相比之下,在7名严重患者的亚组中,M1上的TMS引起了缓慢的、强烈简化的、高振幅的双相反应。这个大的波形持续了约100ms,进一步的TMS锁定活动几乎消失。此外,诱发活动仅局限于患侧M1刺激部位下。
这些不同的TMS-EEG反应模式,即简单的双相模式和更具差异性的模式,也可以在没有诱发MEP的患者亚组中被识别(图2)。因此,TMS-EEG能够揭示无残余运动功能并严重破坏皮质脊髓完整性的患者的不同运动皮层特性,如MEP缺失。
卒中与早期TMS-EEG反应相关
为了量化健康参与者与患者之间以及患者亚组(轻度、中度、重度)之间的差异,我们首先比较了TMS-EEG反应的LMFP对涉及高振幅特征的刺激患侧运动区的影响。结果发现,与健康对照组相比,卒中患者的脑电反应较大,有统计学差异。组间t检验显示,卒中患者在持续到100ms的早期具有较高的TMS诱发反应,但在刺激后的晚期则没有组间差异(图3)。当根据患者最初的运动障碍将患者分为重度、中度和轻度影响组时,这一发现也同样明显。尤其是重度和中度脑卒中患者刺激后早期TMS诱发活动明显高于健康对照组。
与健康对照组相比,患者表现出更多的简单TMS反应。按损伤分组时也检测到组间差异。事后检验显示,与健康对照组相比,重度损伤组患者对TMS的皮层反应更为简单。

图3 通过LMFP对患侧运动区的TEP进行比较
(A)1例典型脑卒中患者和1例健康对照参与者的TMS诱发EEG反应的所有通道(粗体通道代表感兴趣区)的蝶形图;
(B)相应的LMFP,具有两个相应的时间间隔(10-100ms;100-200ms)。
(C)健康参与者和卒中患者组的LMFP条形图。
(D)所有卒中患者和健康参与者的总平均LMFP。虚线表示TMS脉冲的定时。
卒中后早期TMS诱发振荡的主要频率发生改变
为了捕捉脑卒中患者TMS诱发脑电反应的慢特征,我们从TMS患侧M1的三个皮质部位提取了TMS诱发脑震荡活动的主频:患侧前额叶、运动区和顶叶皮质。对排列的秩变换数据进行重复测量的方差分析显示,部位(三个水平:前额叶、运动区、顶叶)´分组(两个水平:患者、对照组)的交互作用显著,表明不同解剖区域诱导的固有频率存在差异。事后检验显示,健康参与者和卒中患者在前额叶和运动区有显著差异,但在顶叶区域没有显著差异。健康对照组在rostral有更多的更高频率的前后梯度,在枕区出现更多的低频振荡。ERSP(事件相关频谱扰动)分析证实,卒中患者的运动和前额叶区域也有慢频谱特征(图4)。此外,患者亚组间的这些差异也很明显。受影响严重的患者表现为与前额叶和运动区的TMS相关的皮层反应迟缓。
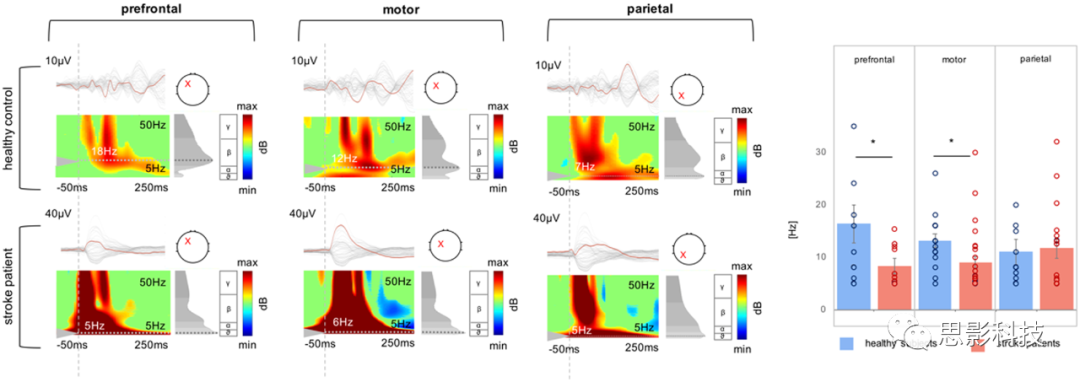
图4 使用ERSP比较固有频率
一名典型卒中患者和一名健康对照参与者的TMS诱发脑电反应,如蝴蝶图所示。蝴蝶地块中的红色通道突出了感兴趣的区域,即前额叶、运动区和顶叶。相应的ERSP模式(在5至50 Hz之间)在其下方。请注意,红叉表示ERSP分析的感兴趣区域,而不是刺激部位,因为刺激部位通常是患侧运动皮质。每个ERSP右侧绘制的灰度图显示了TMS发作后20-200ms期间的功率谱分布。虚线表示功率最大的频率,即固有频率。右侧面板显示每个分析区域的平均固有频率条形图。
运动诱发电位、初始损伤和恢复
总的来说,患者通过NIHSS的降低和所有行为评分的增加,经历了实质性的康复。值得注意的是,严重损害组(n=14)中所有MEP阴性的患者,也表现出恢复。这14名患者中有9名(64.3%)表现出某种程度的康复。
初始运动综合评分与RMT呈负相关,与MEP波幅呈正相关。因此,更严重的运动障碍与更高的RMT和更低的MEP振幅有关。然而,这两个参数都与运动恢复无关,也与MEP阴性的患者(28例中的16例)中的NIHSS指数的一般恢复无关。重要的是,当使用MEP状态,即MEP的存在或不存在,而不是MEP幅度时,产生类似的结果。同样,线性回归分析显示,仅对于MEP阳性患者的子集,MEP振幅与初始运动综合评分相结合可以解释综合运动恢复评分观察到的方差的81.8%。相比之下,当考虑所有卒中患者时,相同的模型未能预测康复。因此,尤其是严重功能障碍和MEP缺失的患者,其恢复情况无法预测。
TMS-EEG初始损害及恢复的关系
我们测试了观察到的TMS诱发脑电活动的改变是否与卒中的初始损害或运动恢复3个月后有关。在卒中后早期,患侧M1低频振荡的TMS-EEG显著改变和偏转的数目与最初的运动障碍有关(图5A)。因此,根据运动综合评分,分化程度较低且频率较低的EEG反应与较强的运动功能障碍相关。此外,第一次检查时的NIHSS分数也发现了这两种相关性。
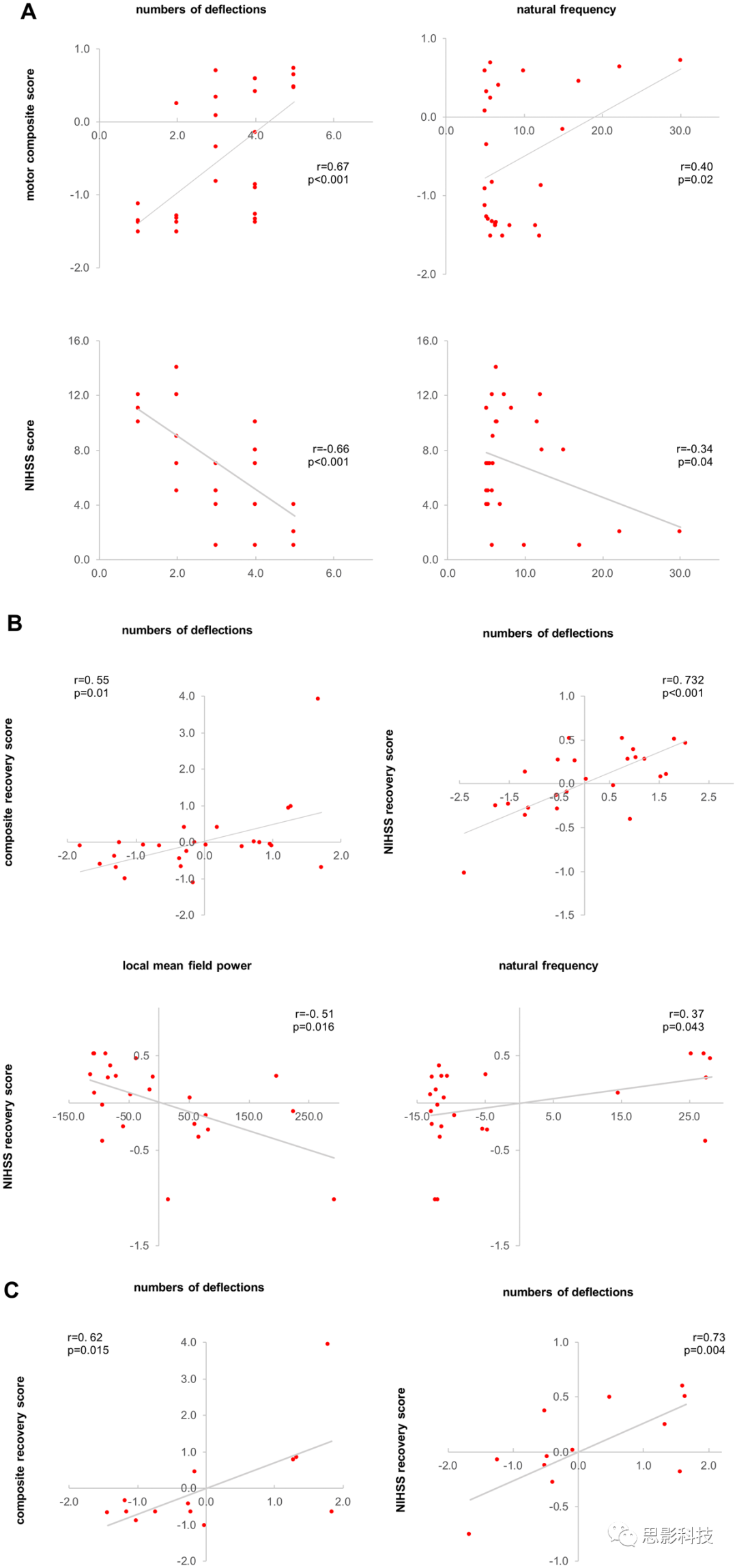
图5 相关分析
我们随后测试了TMS诱发EEG和恢复之间的关系。我们发现卒中后最初几天评估的脑电反应的偏转次数与综合康复评分所反映的较好的运动恢复之间存在正相关。在卒中后的最初几天,以简单、缓慢、振幅高的TMS诱发反应为特征的患者表现出较差的神经学结果。重要的是,TMS-EEG特性与康复之间的这种联系在临床和电生理MEP阴性和严重损害组中得到了证实,进一步强调了TMS-EEG在卒中患者中的有效性。
对于所有卒中患者,以综合康复评分作为结果变量,以初始运动综合评分作为唯一预测因子的线性回归分析显示,初始损伤只能解释11.1%的方差。相比之下,将TMS-EEG参数(LMFP、偏转次数和患侧M1的固有频率)作为自变量加入到模型中,分析表明51.7%的方差可以解释。值得注意的是,如前所述,使用初始运动综合评分和MEP波幅的等效模型在我们的脑卒中患者队列中没有产生对综合运动恢复评分的显著预测。
脑卒中病灶的影响
个别病灶位于基底神经节,即内囊、壳核后肢及丘脑部分部位(图6)。
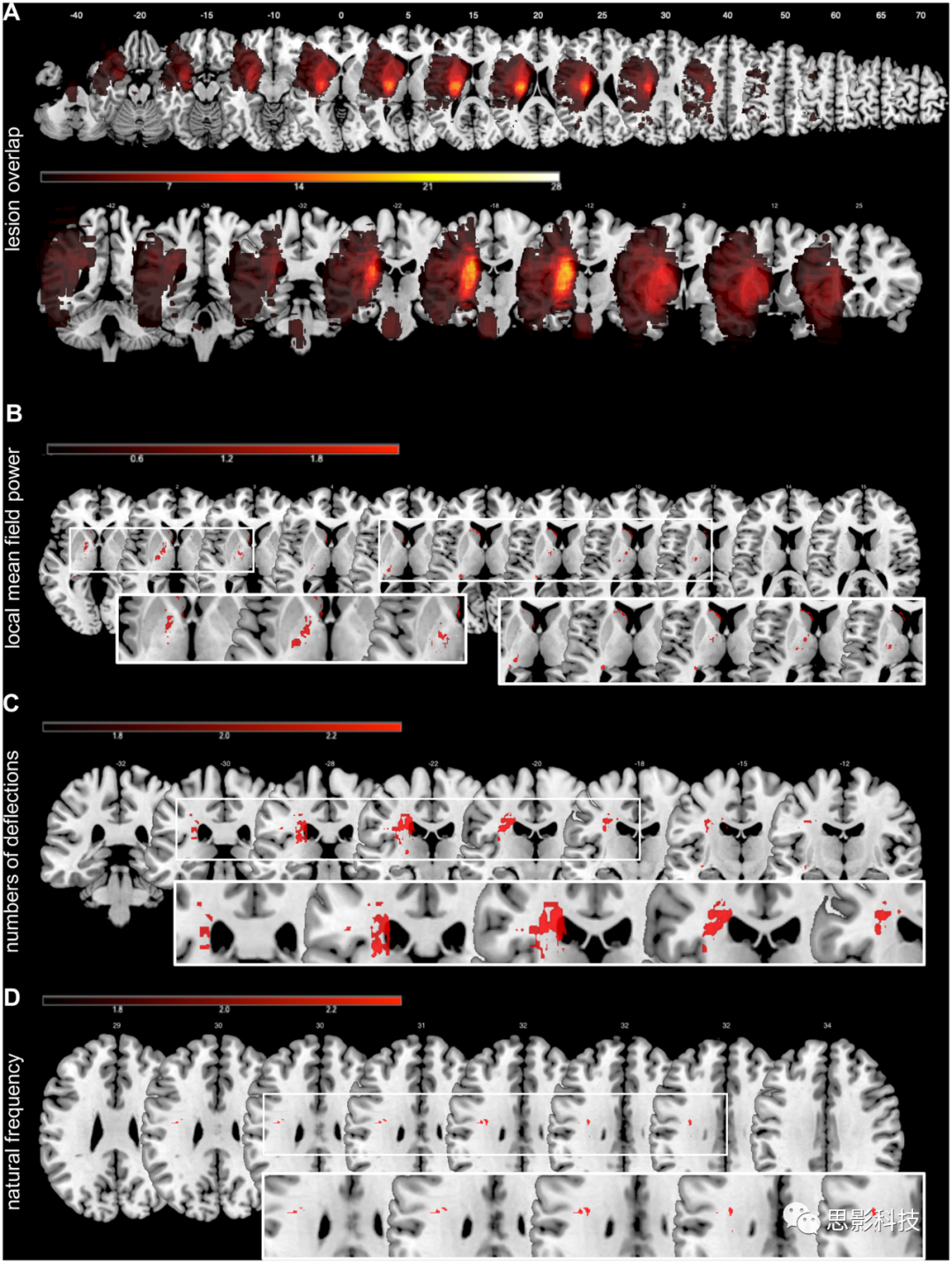
图6 VLSM病灶
(A)脑卒中患者最大病灶位于基底神经节。
(B)与TMS诱发的早期增强LMFP相关的病灶。
(C)与TMS-EEG反应偏转次数减少有关的病灶。
(D)与固有频率变化相关的病灶。
损伤体积与TMS诱发的EEG反应无关,也与中风引起的脑损伤和随后的恢复无关(p值均> 0.2)。相比之下,增强的早期TMS诱发的EEG活动(LMFP)的VLSM显示与内囊和尾状核的病变有关(P<0.05,FDR在体素水平矫正)。相比之下,单纯的TEP模式和固有频率的降低与放射冠皮层下白质的病变有关(P<0.01, FDR校正)(图6)。因此,慢波特征主要与皮质脊髓束的病变有关。因此,中风引起的脑电反应的改变似乎与连接受损而不是M1神经元的主要功能障碍有关。
总结:
作者在28名不同损伤程度的脑卒中和15健康参与者之间的TMS-EEG实验中,使用LMFP(局部平均场功率)、偏转次数和患侧M1的固有频率等指标,测试了TMS-EEG评估卒中后运动恢复的潜力,并探测其余损伤恢复之间的关系。结果发现,TMS-EEG能够探测到不同损伤程度的脑卒中患者的皮层特性,卒中后最初几天评估的脑电反应的偏转次数与综合康复评分所反映的较好的运动恢复之间存在正相关,本研究为脑卒中研究提供新的思路。

微信扫码或者长按选择识别关注思影
如对思影课程感兴趣也可微信号siyingyxf或18983979082咨询。觉得有帮助,给个转发,或许身边的朋友正需要。请直接点击下文文字即可浏览思影科技其他课程及数据处理服务,欢迎报名与咨询,目前全部课程均开放报名,报名后我们会第一时间联系,并保留名额。
第十四届磁共振脑网络数据处理班(重庆,7.26-31)
第三十届磁共振脑影像基础班(南京,7.31-8.5)
第十届脑影像机器学习班(南京,6.30-7.5)
第十二届磁共振弥散张量成像数据处理班(南京,6.18-23)
第二十届脑电数据处理中级班(重庆,8.9-14)